通過后包封法在溫和條件下高效包封mRNA的現貨型LNP開發研究
mRNA 因其誘導目標蛋白表達的能力,在個性化醫療和疫苗開發等領域展現出巨大的潛力。眾所周知,mRNA 是一個帶負電的生物大分子,無法自主穿透細胞膜,必須依賴遞送系統才能發揮作用。脂質納米顆粒已被證明是遞送 mRNA 的理想載體,其制備主要依賴微流控乙醇稀釋法。該方法雖然高效,卻需要精確控制乙醇濃度、pH 梯度和混合速率等多種參數,且必須在顆粒形成過程中同步加入 mRNA。一旦 mRNA 序列發生變更,整個工藝流程往往需要重新優化,這一局限性嚴重阻礙了在個性化醫療場景中實現快速響應的能力。
為了簡化 mRNA-LNPs 的制備過程,日本千葉大學聯合東北大學、大阪大學研究團隊近日在 Nano Letters 發表了題為“A post encapsulation method for the preparation of mRNA-LNPs via the nucleic acid bridged fusion of mRNA free LNPs”的研究論文。該研究開發了一種新型現貨型 LNPs(LNPs (RtoU/Liq)),即通過后包封法(post-encapsulation method)將 mRNA 溶液與預先制備的空包的 LNPs(mRNA-free LNPs)混合,在溫和條件下即可實現高效包封。此方法操作簡單,無需復雜的設備。此外,與需要加熱的“凍干即用型 LNPs”相比,該方法避免了加熱對 mRNA 質量的潛在影響,為 mRNA 藥物的開發提供高效且簡便的解決方案。
一、后包封法的流程
后包封法的核心步驟包括:
1、制備空包的 LNPs:利用微流體混合技術將脂質溶液(乙醇中)與酸性緩沖液混合,形成空包的 LNPs。隨后,通過超濾技術將緩沖液替換成 2-(N-morpholino) 乙磺酸(MES)/蔗糖緩沖液,調整 pH 值至 6.0。
2、配置 mRNA 溶液:將合成的 mRNA 溶解在 MES/蔗糖緩沖液中,調整 pH 值至 6.0。
3、混合封裝:將 mRNA 溶液與空包的 LNPs 進行快速渦旋混合,隨后在 37℃ 下孵育 5 分鐘,以促進 mRNA 的吸附和 LNPs 的融合。
4、中和完成:加入 PBS 中和 pH 值,完成封裝過程。
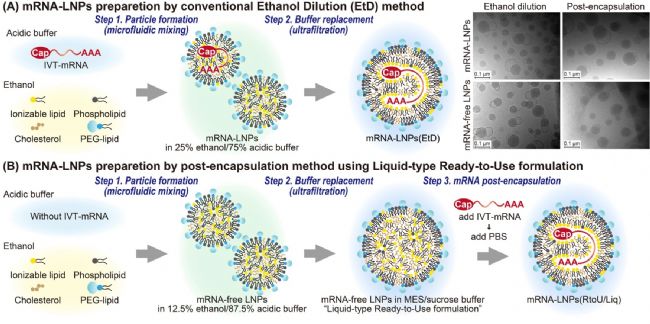
圖1. 兩種包封方法的示意圖
二、后包封法的優化與評估
1、脂質組成的優化
LNP 的核心組分包括可電離脂質、PEG 脂質、磷脂和膽固醇。其中,可電離脂質通過靜電作用與帶負電荷的核酸(如 mRNA)結合,直接影響 mRNA 包封率。研究團隊篩選了三種可電離脂質(DODAP、DLin-MC3-DMA 和 ssPalmO-Phe-P4C2),發現三種脂質在 pH≤6.0 時均能實現超過 70% 的包封率(encapsulation efficiency)。
此外,磷脂分子具有親水頭部和疏水尾部,參與構建 LNP 的穩定結構,可與膽固醇協同提升核酸的包封率。而膽固醇在 LNP 中起到調節膜流動性、穩定性和提高包封率的作用。實驗發現,當膽固醇占比 20%-40% 且磷脂占比 7.5%-20% 時,包封率最高(圖 2)。
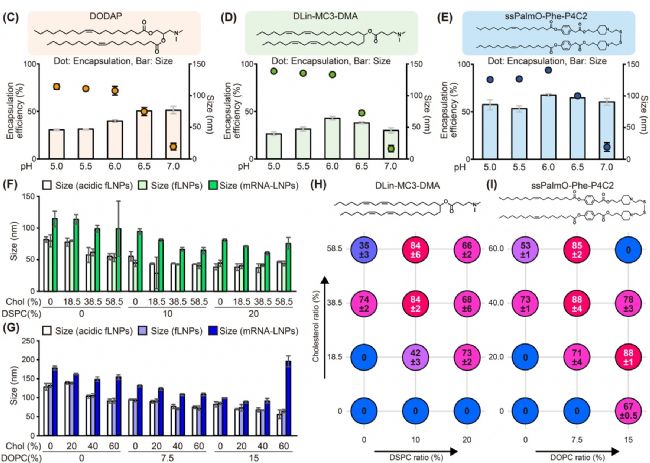
圖2. 脂質組分對包封率的影響
2、mRNA 橋連介導的 LNPs 的融合機制
本研究發現,后包封法(包封率超過 70%)會導致顆粒粒徑顯著增加至原尺寸的 1.27 到 1.78 倍(圖 2H, I)。這種增幅遠超單純 mRNA 封裝所能解釋的范圍,提示存在 LNPs 間的粒子融合。
為了驗證此機制,研究團隊利用納米流式檢測儀(NanoFCM)在單顆粒水平對 mRNA-LNPs 的粒徑和 mRNA 裝載率(loading ratio)進行分析。分別對傳統乙醇稀釋法(EtD)和后包封法(RtoU/Liq)制備的 mRNA-LNPs 進行脂質(DiD)和核酸(SYTO 9)雙重標記,NanoFCM 結果顯示,后包封法的 mRNA 裝載率相比傳統方法提升約 16%(圖 3A-C)。此外,在后包封組中,包封后顆粒的粒徑顯著大于空包的 LNPs(圖 3D),表明在后包封法制備過程中,mRNA 的包封過程中同步發生了顆粒粒徑的增大。
為了進一步驗證 LNPs 之間的融合,研究團隊使用了熒光共振能量轉移技術(fluorescence resonance energy transfer, FRET):將 DiA(熒光供體)與 DiD(熒光受體)共同標記在空包 LNPs 的脂膜上,因二者距離非常接近,發生 FRET,導致 DiA 熒光變弱而 DiD 熒光增強;隨后將雙標記的空包 LNPs 與未標記的 LNPs 以 1:9 的比例混合,加入 mRNA 后,mRNA 通過靜電作用介導“核酸橋連的 LNPs 融合”,原緊密相鄰的 DiA 與 DiD 被未標記 LNPs 的脂質分子分隔,FRET 顯著減弱,DiA 熒光恢復而 DiD 熒光減弱。結果顯示,pH 6.0 條件下 mRNA 可橋接相鄰 LNPs,高效觸發顆粒間的融合(圖 3E-G),從而同步提升包封率和顆粒粒徑。
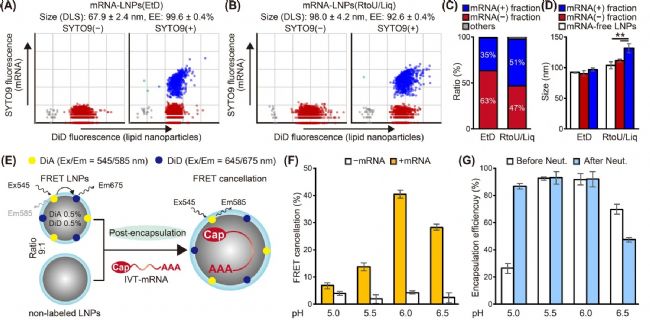
圖3. mRNA 橋連介導的 LNPs 融合驗證
3、LNPs/mRNA 摩爾比優化
接下來,在 pH 6.0 條件下考察 LNPs/mRNA 的摩爾比(L/R比)對后包封法包封率的影響。如圖 4 所示,當 L/R 比低于 50 時,包封率顯著下降;增加 mRNA 相對含量(即降低 L/R 比)會增強 FRET 消除效應并增大顆粒尺寸。進一步通過電泳分析 mRNA 狀態,發現在 L/R 比為 100 的情況下,mRNA 包封率高達 81%,僅有 11% 的核酸被檢測為游離 mRNA;而在 L/R 比為 25 的樣品中,包封率降至 0%,62% 的核酸被檢測為游離狀態,剩余的 38% 在表面活性劑溶解顆粒后被釋放。這一結果表明在低 L/R 比條件下,大部分未包封的 mRNA 以游離形式存在,另有部分 mRNA 可能僅吸附在 LNPs 脂質復合物表面而未被有效包裹。充分說明合適的 L/R 比對于 mRNA 高效吸附于 LNPs 表面并實現穩定封裝至關重要。
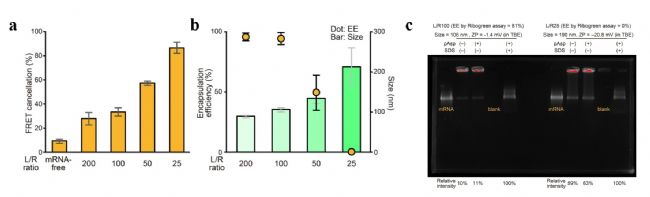
圖4. L/R 比對包封率的影響
4、混合條件的優化
混合條件對包封率也有顯著影響。研究中比較了快速混合(渦旋混合)和慢速混合(輕柔移液)兩種方法。結果表明,快速混合能夠提高包封率,尤其是在高 L/R 比下。這是因為快速混合避免 mRNA 在 LNPs 表面的局部過載,從而避免 LNPs 表面過度吸附 mRNA,導致融合過程受阻。相反,慢速混合會導致 mRNA 局部濃度過高,阻礙顆粒融合進程。
綜上所述,后包封法的效率由 pH 值、脂質組成、L/R 比及混合動力學協同調控。通過優化這些參數,可實現 mRNA 的高效包封,為開發高效、簡便的 mRNA-LNPs 制備工藝提供了重要技術參數。
三、現貨型 LNPs 的 mRNA 遞送效率
接著研究團隊對現貨型 LNPs 遞送 mRNA 的效率進行評估。研究團隊分別采用經典乙醇法和后包封法制備了包封編碼熒光素酶基因的 mRNA-LNPs,分別注射至小鼠體內,活體成像顯示,兩種類型的 mRNA-LNPs 在肝臟中均實現了超過 98% 的選擇性基因表達(圖 5B, C),這表明現貨型 LNPs 在體內遞送 mRNA 方面與傳統方法效果高度一致。
此外,利用后包封法制備包封雞卵清蛋白和新冠病毒刺突蛋白 mRNA 的 LNPs,經小鼠肌肉多次注射,誘導出強效且持久的 IgG 抗體應答(圖 5E)。表明現貨型 LNPs 可應用于 mRNA 疫苗的快速開發。
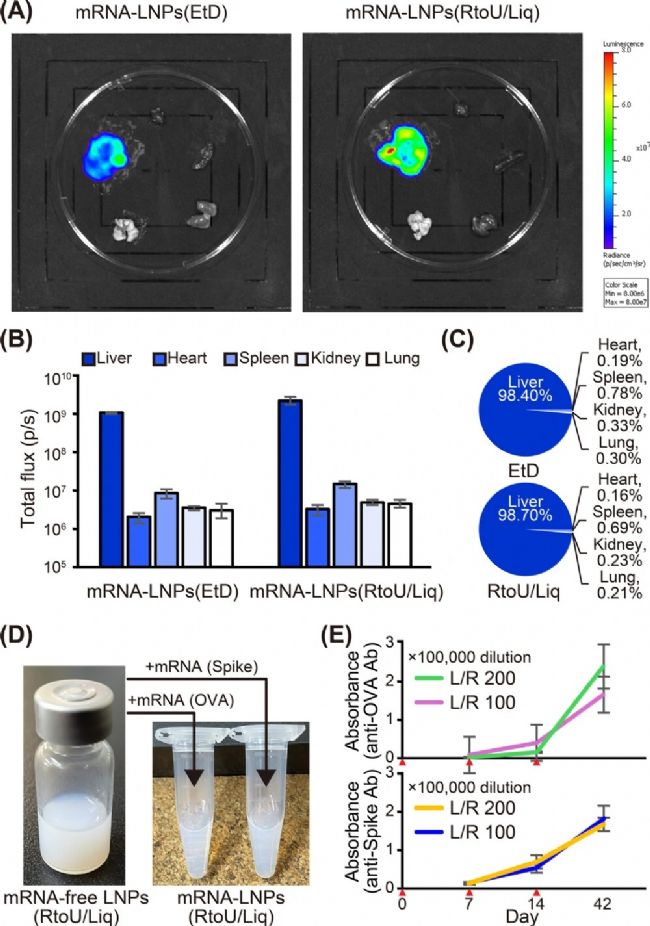
圖5. 現貨型 LNPs 的 mRNA 遞送效率評估
總結與展望
本研究開發了一種基于現貨型 LNPs 的 mRNA 包封新策略,通過核酸橋接融合的方式將 mRNA 高效封裝到預先準備好的 LNPs 中,實現一步反應制備高質量的 mRNA-LNPs。此外,體內外實驗證實,后包封法的基因遞送效率與經典的乙醇稀釋法相當。該方法操作簡單,無需復雜的設備,且省去了傳統凍干工藝的加熱環節,保障了 mRNA 的質量。因此,后包封法為 mRNA 藥物的開發提供了一種高效、簡便的解決方案,具有廣泛的應用前景,有助于加速 mRNA 治療和疫苗開發。
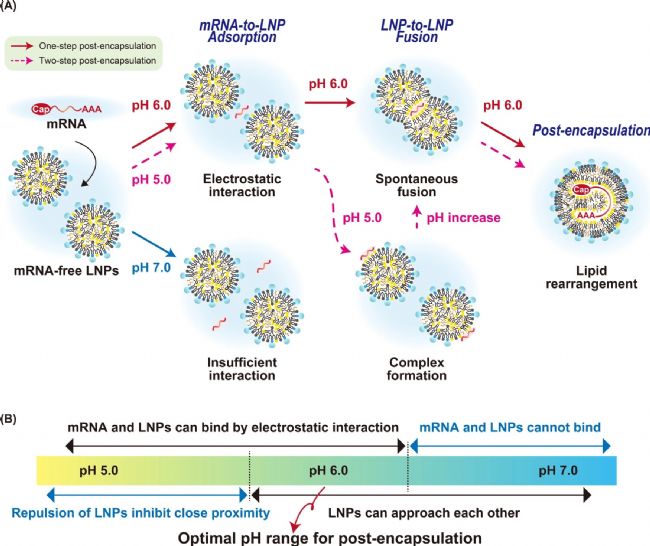
圖6. 后包封法工藝流程圖
NanoFCM 憑借其超高的靈敏度和完善的解決方案,可在單顆粒水平對 mRNA-LNPs 的粒徑分布和封裝率進行評估。通過熒光標記,NanoFCM 能夠精準區分裝載 mRNA 的和空包的 LNPs 顆粒,從而精確計算封裝率。同時,基于單顆粒的散射光強度分析粒徑,發現成功包封 mRNA 后顆粒粒徑顯著增大,揭示 mRNA 封裝與粒徑增大緊密相關,為核酸橋接融合機制提供直接的證據,進一步驗證了后包封法的高效性和可靠性,為優化封裝條件提供了關鍵依據。






