從細菌到大腦:解析大腦-腸道-微生物組軸中的GABA信號網絡

本文基于鄧迪大學delia belelli團隊于BRAIN上發表的一篇名為“From bugs to brain: unravelling the GABA signalling networks in the brain–gut–microbiome axis”的文章進行解讀,其核心目的是系統梳理 γ- 氨基丁酸(GABA)在腦 - 腸 - 微生物組(BGM)軸中的信號傳導網絡,明確其在多系統穩態調節中的作用機制,并為相關疾病的治療提供理論依據與研究方向,具體可拆解為以下 3 點:
1.厘清 GABA 的跨系統整合機制
明確 GABA 如何作為 BGM 軸的 “通用化學信使”,介導大腦、腸道及微生物群之間的雙向通訊,整合分子層面(如受體亞型)與功能層面(如神經元抑制、腸道動力)的離散系統,維持機體整體穩態。
2.解析 GABA 紊亂的病理關聯
闡明 BGM 軸內 GABA 信號異常(如微生物 GABA 合成不足、受體亞型表達失衡)與多系統疾病(胃腸道疾病、精神疾病)的因果關系,解釋疾病 “多器官受累” 的機制,例如女性胃腸道紊亂高發與 GABA 能調節性別依賴性的關聯。
3.提出領域研究與治療方向
基于現有證據缺口,確定 BGM 軸中 GABA 研究的優先級(如功能通路解析、新型配體挖掘),同時為疾病治療提供 “腸道靶向”“亞型特異性” 等創新思路,推動基礎研究向臨床轉化。
研究方法
1.文獻與數據庫系統分析
系統檢索跨物種(人、小鼠、大鼠)BGM 軸研究文獻,覆蓋神經科學、微生物學、免疫學等領域;利用 Protein Atlas 等轉錄組數據庫,分析人類腦與腸道中 GABA_A 受體(GABA_AR)亞基的表達重疊性,識別腸道中功能關鍵但研究較少的亞基(如 ε、ρ 亞基)。
2.已發表數據二次挖掘與可視化
對單細胞 RNA 測序(scRNA-seq)數據(如迷走神經背側運動核(DMV)膽堿能神經元、腸神經系統(ENS)細胞)進行重新分析,解析不同細胞群中 GABA_AR 亞基的表達差異;通過 Heatmapper 生成人類各組織 GABA_AR 亞基表達熱圖(圖 1B),利用 BioRender 構建 BGM 軸信號通路圖(如腦 - 腸神經元連接圖 2、腸道 GABA 作用靶點圖 3),直觀呈現核心機制。
3.跨學科機制推導與模型構建
結合神經藥理學(GABA 受體功能)、微生物代謝學(細菌 GABA 合成通路)、免疫調控理論,推導外周 GABA 影響腦功能的機制(如外泌體介導的遠程通訊);構建 “GABA - 微生物群 - 疾病” 關聯模型,明確擬桿菌屬等 GABA 產生菌與抑郁癥的潛在聯系(圖 4B)。
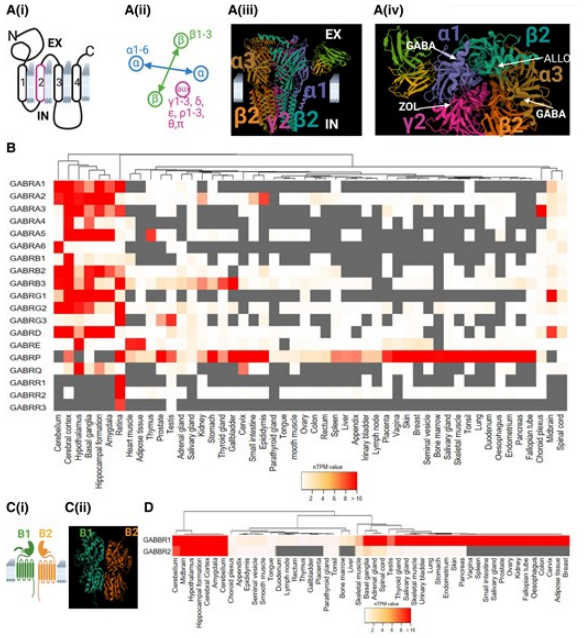
圖1 全身哺乳動物GABA受體的分子、藥理及表達多樣性
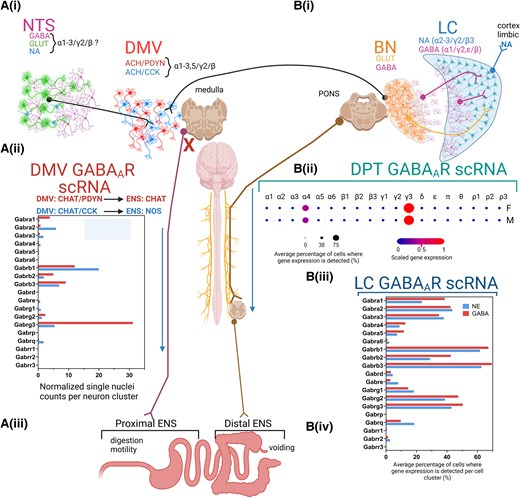
圖2 GABA能信號在腦至腸道神經元通路中的作用
研究內容
1.GABA 與 BGM 軸的基礎分子機制
GABA 受體亞型的多樣性與功能分工:GABA 作用依賴兩類受體 —— 離子型 GABA_AR 與代謝型 GABA_BR。GABA_AR 為五聚體復合物,由 19 種亞基(6α、3β、3γ、δ、ε、θ、π、3ρ)組成(圖 1A (i)(ii)),不同亞基組合決定其功能:含 γ2 亞基的受體對苯二氮䓬類敏感,介導突觸快速抑制;含 δ 亞基的受體位于突觸外,介導持續性緊張性抑制;含 ρ 亞基的受體(原稱 GABA_C 受體)對荷包牡丹堿不敏感,參與腸道收縮調節(圖 1A (iv))。GABA_BR 結構簡單,僅需 GABA_B1(結合 GABA)與 GABA_B2(介導胞內信號)兩種亞基,在腦與腸道中均調節突觸前遞質釋放(圖 1C、D)。
GABA 的雙向信號傳導路徑:BGM 軸中 GABA 信號呈 “自上而下” 與 “自下而上” 雙向傳遞。“自上而下” 路徑中,大腦通過 DMV、藍斑核(LC)、巴林頓核(BN)等核團調節腸道功能(如 DMV GABA_AR 激活抑制胃動力,圖 2A (i));“自下而上” 路徑中,腸道神經元、免疫細胞、微生物產生的 GABA,通過迷走神經傳入、免疫介質擴散、外泌體運輸影響腦功能(如腸道 GABA 激活迷走神經末梢受體,圖 5A)。
2.不同組織中 GABA 的功能作用
大腦中 GABA 的功能:作為中樞主要抑制性神經遞質,GABA 通過調節神經元興奮性控制胃腸道相關腦區活動(如 DMV 神經元),且調節具有性別依賴性 —— 高雌激素階段雌性大鼠的 DMV GABA 能抑制更強,可能導致女性胃腸道紊亂高發(圖 2A (i));同時,GABA 通過調節默認模式網絡連接性影響情緒,如擬桿菌屬豐度與抑郁癥患者默認模式網絡連接性負相關。
腸道中 GABA 的功能:腸道 GABA 由腸神經元、腸膠質細胞、腸內分泌細胞(如腸嗜鉻細胞)及微生物產生,通過 ENS 調節腸道功能(圖 3A (iii)):含 ρ 亞基的 GABA_AR 調節小鼠回腸慢抑制電位,α3-GABA_AR 參與壓力誘導的結腸炎癥(圖 3B (ii)(iii));GABA 還可激活腸嗜鉻細胞受體,促進 5 - 羥色胺釋放,間接傳遞腸道感覺信號。
微生物群中 GABA 的功能:腸道微生物(擬桿菌屬、乳桿菌屬、雙歧桿菌屬)通過谷氨酸脫羧酶(GAD)途徑合成 GABA(圖 4A),產生濃度(0.09-60.84 mM)處于生理活性范圍;微生物 GABA 可調節自身群落平衡(如作為營養物質或毒力抑制劑),還能通過影響腸道 GABA 水平改善腦功能,如卵形擬桿菌定植可增加海馬體腦源性神經營養因子,緩解抑郁表型(圖 5D)。
3.GABA 與其他 BGM 軸信使的相互作用
GABA 與短鏈脂肪酸(SCFAs)的協同作用:SCFAs(如乙酸鹽)可穿過血腦屏障,參與神經元 GABA 合成(約 30%);反之,GABA 可增加小鼠盲腸 SCFAs 含量,兩者共同參與益生菌(如地衣芽孢桿菌)的抗抑郁作用 —— 乙酸水平與 GABA 呈正相關,協同改善抑郁樣行為。
GABA 與 5 - 羥色胺(5-HT)的調控軸:腸道 95% 的 5-HT 由腸嗜鉻細胞產生,而腸嗜鉻細胞表達 GABA_AR 與 GABA_BR,GABA 可直接調節 5-HT 釋放;微生物通過 SCFAs 上調腸嗜鉻細胞 5-HT 合成酶(TPH1)表達,GABA 則通過影響 SCFAs 間接調控 5-HT 水平,形成 “GABA-SCFAs-5-HT” 調控軸(圖 5B)。
4.GABA 紊亂與疾病的關聯
胃腸道疾病:腸易激綜合征(IBS)患者存在腸道 GABA 能信號失調(如 GABA_AR 亞型表達異常),導致腸道動力障礙與炎癥;壓力誘導的腸道屏障破壞也與 α3-GABA_AR 介導的炎癥相關(圖 3B (iii))。
精神疾病:抑郁癥、焦慮癥、自閉癥患者中,腸道 GABA 產生菌(如擬桿菌屬)豐度降低,微生物 GABA 合成減少,同時大腦 GABA 能抑制缺陷;酒精使用障礙患者的腸道菌群失調,微生物 GABA 紊亂可能加重焦慮、抑郁等共病癥狀(圖 4B)。
5.未來研究方向與治療策略
基礎研究優先級:明確腸神經系統中神經元釋放 GABA 調節腸道功能的直接證據(如 GABA 介導的突觸后電位);利用基因修飾小鼠離散操縱外周器官 GABA_AR 亞基表達,解析其多系統功能;通過計算機配體 - 受體對接,結合細菌代謝組學數據,挖掘 GABA_AR 新型內源性配體。
治療策略設計:開發 GABA 相關飲食干預,如補充含 GABA 產生菌的益生菌(乳桿菌屬、雙歧桿菌屬)、促進微生物 GABA 合成的益生元(人乳低聚糖、低聚果糖,圖 5D (i));靶向特定 GABA_AR 亞型開發藥物,如 α2/3-GABA_AR 選擇性激動劑(抗焦慮且無鎮靜作用)、ε-GABA_AR 配體(調節全身穩態)。
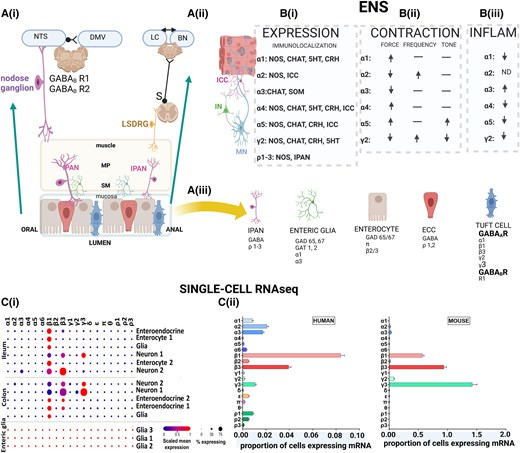
圖3 GABA能信號在神經元及非神經元腸道至大腦通路中的作用
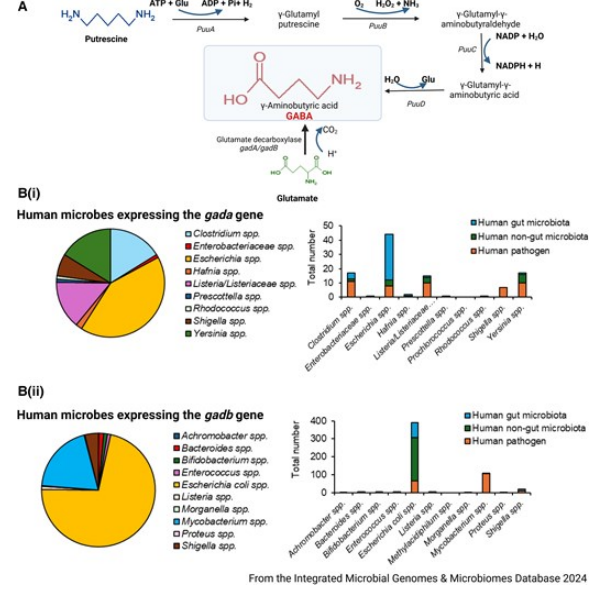
圖4 細菌GABA合成
構建 “GABA 跨系統信號網絡” 新框架:首次系統整合大腦、腸道、微生物群中 GABA 的作用,打破 “GABA 僅為中樞抑制遞質” 的認知,明確其在微生物群調節(細菌群落平衡)、免疫調控(抑制結腸炎癥)、代謝交互(與 SCFAs/5-HT 協同)中的新型功能,建立多系統聯動的 GABA 信號模型(圖 5)。
聚焦 “外周 GABA 的腦調節機制” 研究缺口:以往研究多關注大腦 GABA,本文重點解析外周(腸道、微生物群)GABA 影響腦功能的三類關鍵機制 —— 腸神經系統 GABA 激活迷走神經傳入、免疫細胞 GABA 調節全身炎癥、腸道 GABA 誘導外泌體遠程通訊(圖 5A、B、C),首次證實微生物 GABA 可通過 “腸道 - 免疫 - 腦” 路徑影響情緒,為精神疾病 “腸道靶向治療” 提供理論依據。
建立 “GABA 受體亞型 - 組織功能 - 疾病” 精準關聯:通過整合轉錄組數據與功能研究,明確不同 GABA_AR 亞型的組織特異性功能與病理意義(圖 1B、3B):ε 亞基在下丘腦與外周器官均高表達,參與全身穩態協調;ρ 亞基在腸道調節收縮性,與 IBS 相關;α3 亞基介導壓力誘導的腸道炎癥,與焦慮共病相關,為 “亞型特異性靶向治療” 奠定基礎,避免傳統藥物的非特異性副作用。
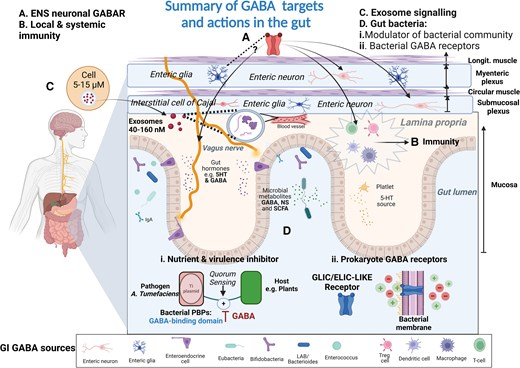
圖5 GABA在胃腸道中的多樣化來源、作用和靶點
我們應該關注 “腸道 - 腦” 日常維護
通過飲食維持腸道 GABA 穩態:日常可增加富含益生元的食物(菊粉、洋蔥、香蕉),促進 GABA 產生菌生長;適量攝入發酵食品(GABA 酸奶、納豆),直接補充外源性 GABA,間接保護腦功能,降低焦慮、抑郁風險。
重視 “腸道 - 情緒” 關聯信號:胃腸道紊亂與精神疾病常共病(如 IBS 患者焦慮發病率高),臨床需關注 “腸道不適伴情緒異常” 患者,評估其腸道功能(動力、炎癥)與 GABA 相關指標(糞便 GABA 水平、微生物組成),避免單一治療導致療效不佳。
我們應該關注 “腸道 - 腦” 日常維護
通過飲食維持腸道 GABA 穩態:日常可增加富含益生元的食物(菊粉、洋蔥、香蕉),促進 GABA 產生菌生長;適量攝入發酵食品(GABA 酸奶、納豆),直接補充外源性 GABA,間接保護腦功能,降低焦慮、抑郁風險。
重視 “腸道 - 情緒” 關聯信號:胃腸道紊亂與精神疾病常共病(如 IBS 患者焦慮發病率高),臨床需關注 “腸道不適伴情緒異常” 患者,評估其腸道功能(動力、炎癥)與 GABA 相關指標(糞便 GABA 水平、微生物組成),避免單一治療導致療效不佳。
參考文獻:
Ma T, Liu J, Gao Z, Li Y, Lin J, Pang K, Li R, Zhang X, Tang L, Liu Y, Zhang H, Zhang Y, Cai LC, Zhou Z, Shi K, Zhu T, Zhang J, Chen J, Cai Z, Fu Y, Zhao Z. Bone marrow-derived emergency monopoiesis drives brain-lung axis injury after traumatic brain injury via IL-1. J Neuroinflammation. 2025 Nov 5;22(1):262. doi: 10.1186/s12974-025-03589-yIF: 10.1 Q1 . PMID: 41194087; PMCID: PMC12590780.
創作聲明:本文是在原英文文獻基礎上進行解讀,存在觀點偏向性,僅作分享,請參考原文深入學習。


想了解更多內容,獲取相關咨詢請聯系
電 話:+86-0731-84428665
伍經理:+86-180 7516 6076
工程師:+86-180 7311 8029
郵 箱:consentcs@163.com







