骨髓來源的緊急單核細胞通過IL-1驅動TBI后腦肺軸損傷的研究

創傷性腦損傷(TBI)是全球性的健康危機,其危害遠不止于急性神經功能缺損,常伴隨嚴重的肺部并發癥,共同構成致命的“腦-肺軸”損傷。盡管這一臨床現象已被廣泛認知,但其背后的機制一直不明,導致缺乏有效的干預手段。本文基于天津醫科大學趙子龍及其團隊等人發表于《Journal of Neuroinflammation》的最新研究,系統闡述TBI如何通過激活白細胞介素-1(IL-1)信號通路,驅動骨髓(特別是顱骨骨髓)發生緊急單核細胞生成,進而導致促炎性免疫細胞向腦和肺組織浸潤,最終加劇多器官損傷的全新病理過程。該研究不僅揭示了腦-肺軸損傷的核心驅動機制,還通過基因敲除和藥物干預實驗,驗證了靶向IL-1R1信號通路作為治療TBI多器官損傷的潛在策略,為改善TBI患者臨床預后提供了新的思路。
一、臨床證據揭示TBI患者顱骨骨髓存在緊急單核細胞生成并與器官損傷相關
研究的起點源于對臨床問題的深入觀察。為了探究TBI急性期造血系統的改變,研究者收集了因嚴重TBI需行去骨瓣減壓術患者的顱骨骨髓樣本,并以因非創傷性疾患(如寰枕畸形)手術患者的骨髓樣本作為對照。通過對骨髓單個核細胞進行高精度的單細胞RNA測序分析,研究發現,與對照組相比,TBI患者的骨髓造血生態發生了顯著重塑。其最突出的特征是髓系細胞的異常活躍,表現為單核細胞、中性粒細胞及其祖細胞群體的比例顯著升高,而相應的干細胞池則有所減少。這提示骨髓正處于一個加速生產髓系細胞的“緊急造血”狀態。更為重要的是,這種骨髓的異常激活狀態與患者的臨床結局密切相關。分析顯示,骨髓中單核細胞群體的擴張程度,與影像學評估的腦損傷嚴重程度(Rotterdam評分)和肺損傷程度(Ichikado評分)均呈現出顯著的正相關性。這一發現首次在人體水平直接將TBI后的骨髓應激反應與遠隔器官(腦和肺)的損傷聯系了起來,為“腦-肺軸”的存在提供了堅實的細胞學證據。
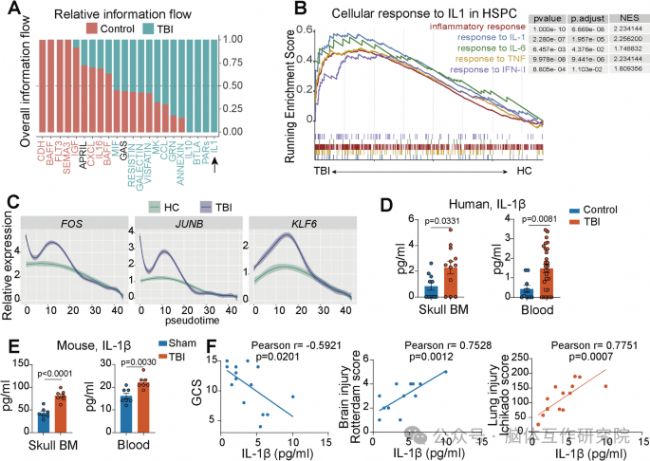
圖1 IL-1 信號傳導在 BM 細胞中顯著上調,并與 TBI 誘導的腦肺損傷相關
二、IL-1信號通路被鑒定為驅動骨髓病理反應的關鍵上游因子
在確認了骨髓緊急單核細胞生成的重要性后,研究者進一步探尋其啟動的關鍵信號。對單細胞測序數據的深入挖掘發現,TBI患者的骨髓細胞,尤其是造血干細胞和祖細胞,表現出強烈的炎癥反應特征。在眾多炎癥信號通路中,IL-1通路的信息流在細胞間通訊中顯著增強,提示其可能扮演著核心角色。偽時間軌跡分析顯示,TBI患者的造血祖細胞高表達一系列促進髓系分化的關鍵轉錄因子,這可能是驅動髓系偏斜的分子基礎。為了驗證這一發現,研究團隊檢測了TBI患者和小鼠模型骨髓及外周血中IL-1β的蛋白水平,結果一致表明,在損傷早期,IL-1β的表達量急劇升高。回歸到臨床意義,分析顯示患者血漿中的IL-1β水平與昏迷評分呈負相關,而與腦、肺損傷評分呈正相關。這些數據層層遞進,共同將IL-1β鎖定為連接TBI原發損傷與骨髓異常造血的一個關鍵信使分子,將其推向了機制研究的中心舞臺
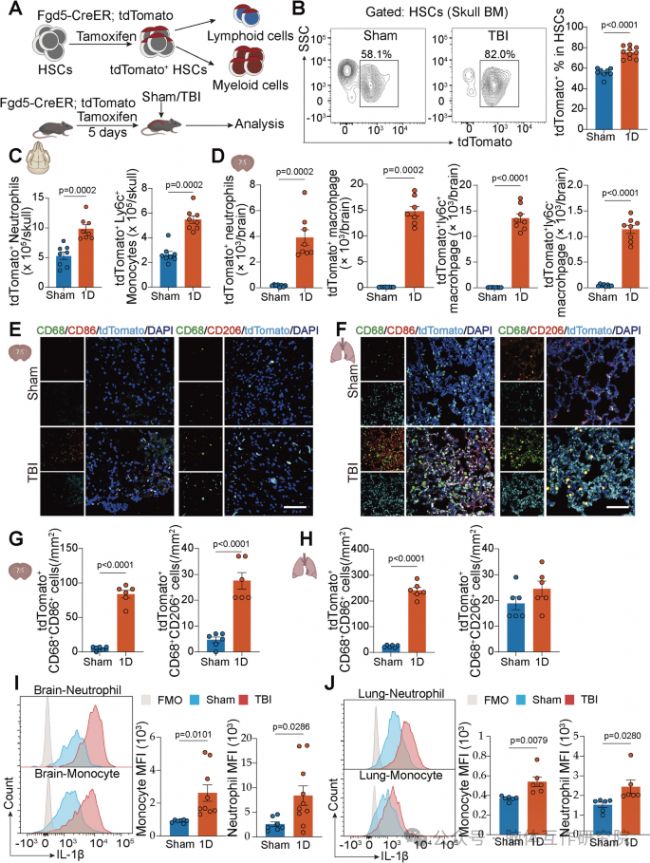
圖2 TBI誘導的BM單生成促進腦和肺損傷
三、動物模型證實骨髓來源的促炎細胞直接浸潤腦與肺并加劇損傷
為了在體內動態追蹤并證實骨髓細胞的命運,研究采用了先進的譜系追蹤小鼠模型。該模型能夠在TBI前特異性標記骨髓中的造血干細胞,從而可以清晰地區分損傷后從骨髓新生成并遷移出去的免疫細胞。利用這一技術,研究直觀地證實,TBI后確實發生了快速的骨髓激活,這些新生的細胞主要為造血干細胞來源。隨后,這些細胞在骨髓內分化為中性粒細胞和單核細胞,并大量涌入外周。更重要的是,在受損的腦組織和原本健康的肺組織中,均發現了大量來自骨髓的tdTomato陽性細胞,其中以具有促炎表型的巨噬細胞和中性粒細胞為主。這些細胞在靶器官中高表達IL-1β等炎癥因子,如同“炎癥炸彈”一般,局部放大炎癥反應,直接破壞血腦屏障和肺泡結構。這套完整的證據鏈,在活體動物水平實現了從“因”(TBI)到“果”(多器官損傷)的閉環論證,明確了骨髓緊急單核細胞生成是腦-肺軸損傷的關鍵中間環節。
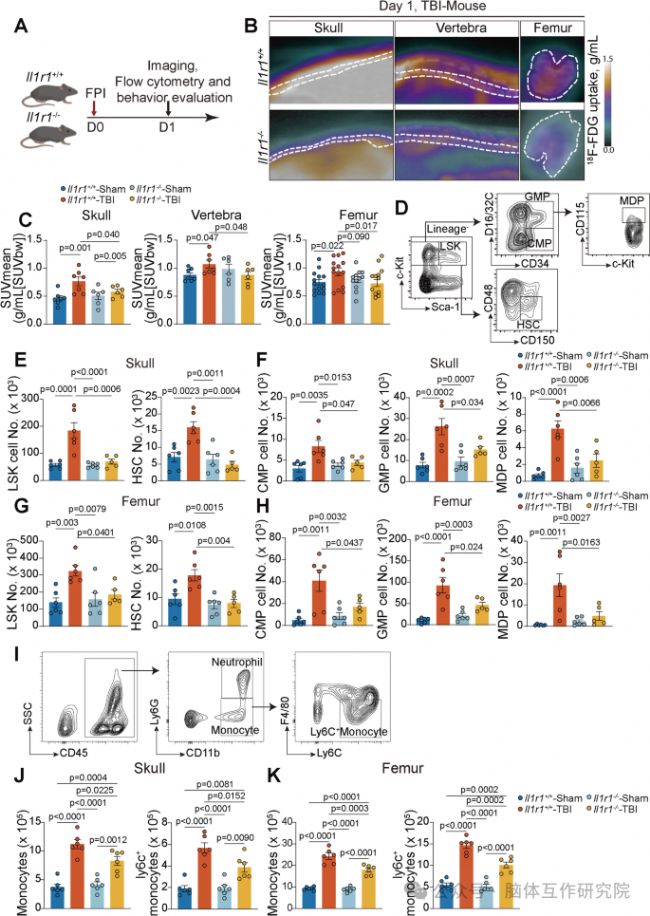
圖3 Il11 的全球損失緩解了 TBI 引起的緊急壟斷
四、基因敲除研究證實IL-1信號是病理性骨髓激活的必要條件
為了確立IL-1信號的因果關系,研究引入了全身性IL-1受體1(IL-1R1)基因敲除(Il1r1-/-)小鼠。PET-CT成像顯示,野生型小鼠在TBI后,其全身多處骨髓(包括顱骨、椎骨、股骨)的代謝活性顯著增強,而這一現象在Il1r1-/-小鼠中被大幅抑制。流式細胞術分析進一步揭示,Il1r1-/-小鼠骨髓中造血干細胞、各類髓系祖細胞以及成熟單核細胞的擴增反應均明顯弱于野生型小鼠。這充分證明,IL-1信號是TBI觸發全身性骨髓緊急單核細胞生成不可或缺的分子開關。由于骨髓反應被抑制,Il1r1-/-小鼠在遭受TBI后,其腦和肺組織內促炎巨噬細胞的浸潤顯著減少。隨之而來的是,一系列積極的保護性效應:磁共振成像顯示腦損傷范圍縮小、血腦屏障泄漏減輕、腦內鐵沉積減少;組織學檢查可見肺內炎癥細胞浸潤和肺泡結構破壞得到改善;肺功能測試和神經行為學評分也一致表明,Il1r1-/-小鼠的肺功能和神經功能均得到更好的保全。這些結果強有力地說明,阻斷IL-1信號可以通過抑制骨髓的病理反應,從而同時減輕腦和肺的繼發性損傷。
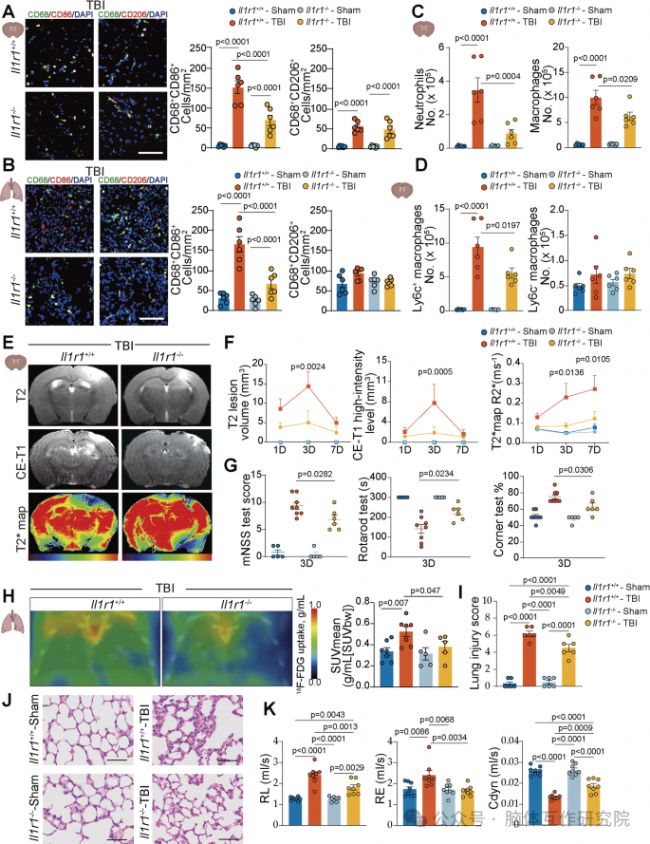
圖4 通過整體失去 Il1r1 來抑制緊急壟斷,減輕了 TBI 引起的腦和肺損傷
五、造血細胞特異性IL-1R1缺失足以模擬全身敲除的保護效應
為了更精確地定位IL-1信號的作用靶點,研究設計了精巧的骨髓嵌合體實驗。通過將Il1r1-/-或野生型小鼠的骨髓細胞移植給經過輻照清髓的野生型受體小鼠,成功構建了僅造血系統缺失IL-1R1信號,而其他組織器官信號完整的小鼠模型。對這類小鼠施加TBI后,觀察到了與全身敲除小鼠高度一致的表型:腦內炎癥細胞浸潤減少,腦損傷和肺損傷均得到顯著緩解。這一關鍵實驗將IL-1信號驅動病理過程的核心作用明確限定在了造血系統本身。它表明,IL-1(可能來源于受損的腦組織或其他部位)主要是通過直接作用于骨髓中的造血細胞(表達IL-1R1),才能啟動后續的惡性循環。這一發現極大地提升了治療策略的精準性,暗示我們或許不需要全面抑制全身的IL-1信號,而只需靶向造血細胞,即可達到治療目的,有望減少潛在副作用。
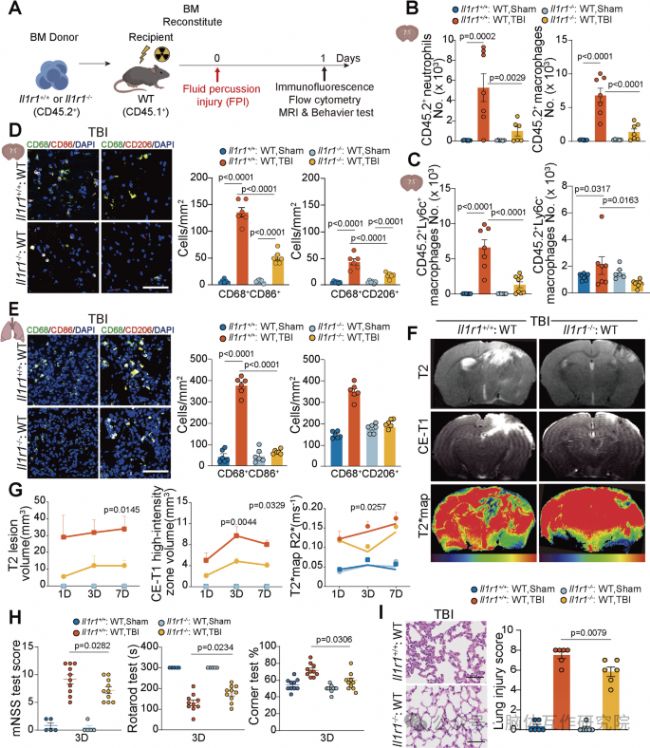
圖5通過造血特異性缺失 Il1r1 抑制緊急單噬,減輕了 TBI 引起的腦和肺損傷
六、IL-1受體拮抗劑阿那白滯素展現出潛在的治療前景
基于上述堅實的機制研究,該工作最終邁向轉化醫學的探索。研究團隊使用了美國FDA已批準的IL-1受體拮抗劑——阿那白滯素(Anakinra)對TBI小鼠進行干預。結果顯示,阿那白滯素治療能夠有效模擬基因敲除的效果,顯著抑制TBI后骨髓的緊急單核細胞生成,減少促炎細胞向腦和肺的遷移。在功能層面,藥物治療組小鼠的腦損傷和神經功能缺損明顯減輕,同時肺部的炎癥浸潤和功能損傷也得到了有效遏制。這一發現具有重大的臨床意義,它表明阿那白滯素作為一種“老藥”,可能具有治療TBI后多器官并發癥的“新用”。由于IL-1信號通路在造血環節的核心地位,靶向該通路有望在抑制神經炎癥的同時,不顯著削弱肺部對抗感染的免疫力,從而規避當前糖皮質激素等非特異性抗炎治療可能增加肺炎風險的困境,為未來開展臨床研究提供了強有力的理論依據和實驗支持。
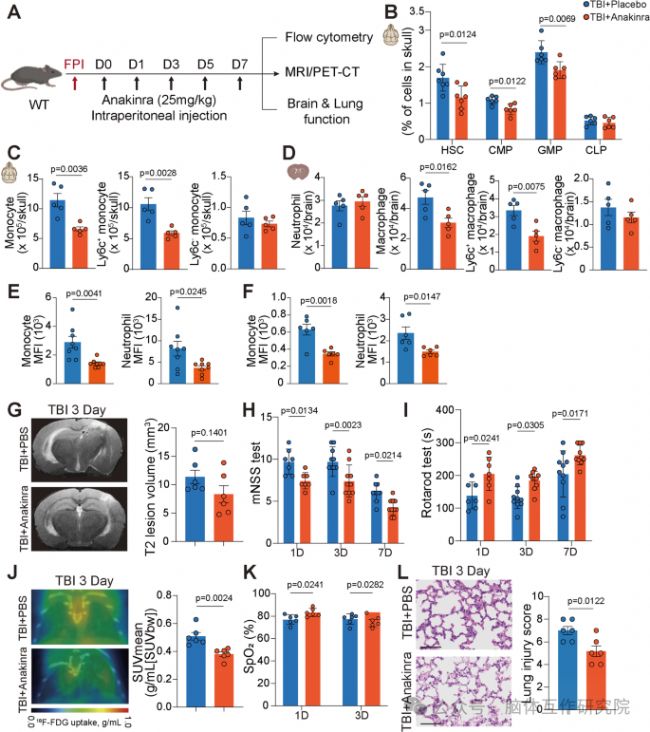
圖6 IL-1R的全身藥理學抑制減少了TBI小鼠的緊急單穿并保護了腦和肺損傷
七、總結與展望
在此文章的研究中,我們認為可以結合穩定、精準的多位點同步微透析采樣,尤其是在肺部等復雜組織環境中,對技術的穩定性和靈敏度提出了極高要求。微透析技術具有重要潛在應用價值:它可用于在體、實時監測TBI后大腦細胞外液(甚至肺部組織液)中炎癥因子(如IL-1β)的動態變化。這一技術能為本研究帶來關鍵的補充價值:首先,它可直接驗證分子機制。本研究通過ELISA和單細胞測序推斷IL-1β是關鍵上游信號,而微透析技術則能在損傷核心區、半暗帶或特定腦區(如調控自主神經的下丘腦)實時監測IL-1β的釋放動力學,為“IL-1驅動”這一核心假設提供更直接的時空動態證據。其次,它有助于揭示腦-肺通訊。通過在腦和肺同時進行微透析采樣,可以更精確地探索炎癥因子從腦部向全身擴散的時程和路徑,為“腦-肺軸”提供更直接的生化證據。
參考文獻:Ma T, Liu J, Gao Z, Li Y, Lin J, Pang K, Li R, Zhang X, Tang L, Liu Y, Zhang H, Zhang Y, Cai LC, Zhou Z, Shi K, Zhu T, Zhang J, Chen J, Cai Z, Fu Y, Zhao Z. Bone marrow-derived emergency monopoiesis drives brain-lung axis injury after traumatic brain injury via IL-1. J Neuroinflammation. 2025 Nov 5;22(1):262. doi: 10.1186/s12974-025-03589-yIF: 10.1 Q1 . PMID: 41194087; PMCID: PMC12590780.
創作聲明:本文是在原英文文獻基礎上進行解讀,存在觀點偏向性,僅作分享,請參考原文深入學習。


想了解更多內容,獲取相關咨詢請聯系
電 話:+86-0731-84428665
伍經理:+86-180 7516 6076
工程師:+86-180 7311 8029
郵 箱:consentcs@163.com







