揭示高血壓損害大腦血管與認知功能的細胞機制研究
2025年11月14日威爾康奈爾醫學院Costantino Iadecola團隊在Neuron雜志發表文章利用單細胞測序技術揭示了早期高血壓中內皮細胞、少突膠質細胞前體細胞及中間神經元是最為敏感的細胞類型。

1、早期高血壓和晚期高血壓引起內皮細胞差異性轉錄組學變化
研究人員發現皮下連續注射低劑量AngII 3天后小鼠血壓開始升高,2周后出現神經血管損傷,6周后存在顯著的認知功能障礙。為揭示神經血管功能障礙如何伴隨認知障礙發生發展,研究人員在注射3天和6周AngII后皮層組織進行單細胞測序,發現AngII引起轉錄組學變化最顯著的細胞類型為內皮細胞、少突膠質細胞譜細胞和神經元。與動脈區內皮細胞相比,靜脈區內皮細胞表現出顯著更多的差異表達基因。
更具體來說,注射3天AngII后皮層毛細血管-微靜脈內皮細胞(vCapEC)和毛細血管內皮細胞(vEC)富集性表達能量穩態信號基因下調,氧化性脂肪酸代謝信號相關信號基因上調,提示存在衰老表型。免疫熒光實驗發現周期蛋白依賴激酶抑制劑p21、p27在vCapEC中表達顯著增加,這種增加可被血管緊張素II 受體拮抗劑所阻斷,表明注射3天AngII后通過其受體引起皮層vCapEC衰老。
注射42天AngII后皮層小動脈內皮細胞出現顯著轉錄組學變化:小動脈-微靜脈內皮細胞(aCapEC)和小動脈內皮細胞(aEC)血管重塑和膠原代謝相關基因表達上調,氧化還原穩態相關基因表達下調。免疫熒光實驗發現注射42天AngII后皮層微血管中的IV型膠原蛋白表達增加,提示血管重塑。
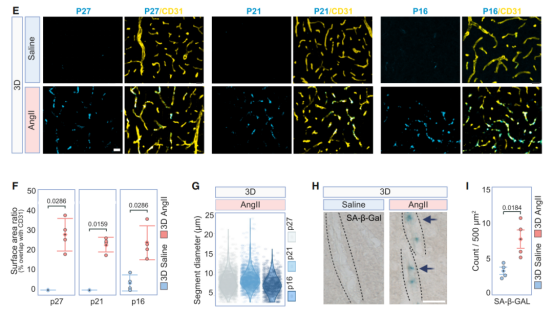
圖1、注射3天AngII后皮層vCapEC衰老
2、早期高血壓和晚期高血壓引起少突膠質細胞差異性轉錄組學變化
注射3天AngII后皮層少突膠質細胞前體細胞(OPCs)與DNA損傷相關的基因表達上調,前體少突膠質細胞的應激反應基因表達上調,成熟少突膠質細胞Neurexin-Neuroligin信號相關基因表達下調。免疫熒光實驗發現OPCs的DNA損傷標志物γ-H2A.X表達上調。注射42天AngII后皮層OPCs與脂肪酸代謝相關的基因表達下調、DNA合成和細胞周期相關的基因表達也下調,而骨形態發生蛋白信號相關基因表達上調,表明OPCs的增殖、合成等過程出現紊亂。
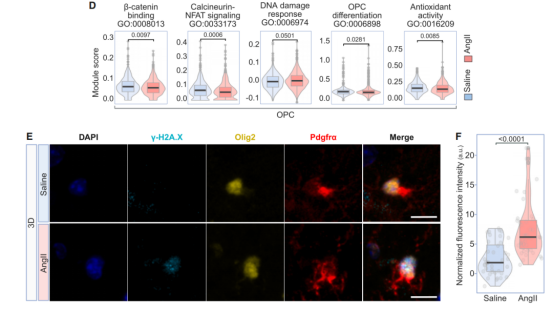
圖2、注射3天AngII后皮層OPCs DNA損傷增多
3、早期高血壓和晚期高血壓引起神經元差異性轉錄組學變化
AngII注射誘導的神經元轉錄組特征呈現出明顯的時間變化特征:中間神經元差異性表達基因數量在注射后3天時達峰,第42天時減少,而該動態模式在興奮性神經元中則未觀察到。
具體來說,注射AngII 3天后皮層中間能神經元氧化還原、細胞應激反應及鉀穩態相關基因表達上調,興奮性神經元突觸功能相關的基因表達上調,表明早期HTN期間中間神經元的突觸功能出現紊亂,同時興奮性神經元的突觸功能增強,即興奮-抑制失衡。注射42天AngII后皮層興奮性神經元與調控突觸組織蛋白和突觸結構相關的基因表達顯著上調,興奮性突觸AMPA受體相關基因表達上調,表明興奮性神經元活動增強。
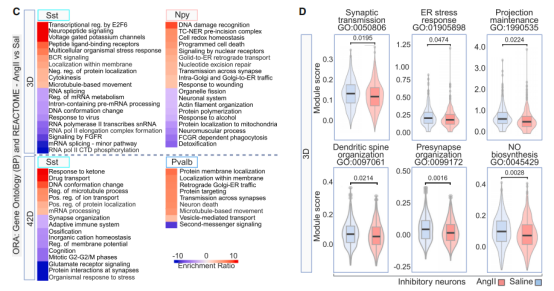
圖3、早期HTN期間中間神經元的突觸功能出現紊亂
總結:
本文利用緩慢發展的高血壓小鼠模型發現在早期高血壓期間引起毛細血管內皮細胞轉運紊亂、細胞衰老,少突膠質細胞前體細胞DNA損傷增強,增殖受損,抑制性中間能神經元功能紊亂,抑制一氧化氮合成;晚期高血壓期間引起小動脈血管重塑,成熟少突膠質細胞合成受損,軸突功能出現紊亂,興奮性神經元活性增強,出現認知功能障礙。
參考文獻:Schaeffer et al., Hypertension-induced neurovascular and cognitive dysfunction at single-cell resolution, Neuron(2025), https://doi.org/10.1016/j.neuron.2025.10.018
創作聲明:本文是在原英文文獻基礎上進行解讀,存在觀點偏向性,僅作分享,請參考原文深入學習。


想了解更多內容,獲取相關咨詢請聯系
電 話:+86-0731-84428665
伍經理:+86-180 7516 6076
工程師:+86-180 7311 8029
郵 箱:consentcs@163.com







