Simoa技術揭示大腦健康與新陳代謝的深層關聯
你是否想過,為什么代謝異常的人更容易患上阿爾茨海默病(Alzheimer disease,AD)?為什么肥胖可能加劇神經炎癥?近年來,科學家們發現,新陳代謝與大腦健康之間存在千絲萬縷的聯系。然而,傳統檢測技術難以捕捉血液或腦脊液中極微量的關鍵分子,使得這一領域的探索充滿挑戰。如今,Simoa(單分子免疫陣列)技術的突破,讓科學家擁有了“分子顯微鏡”,能夠以極高的靈敏度揭示代謝與大腦的深層關聯。
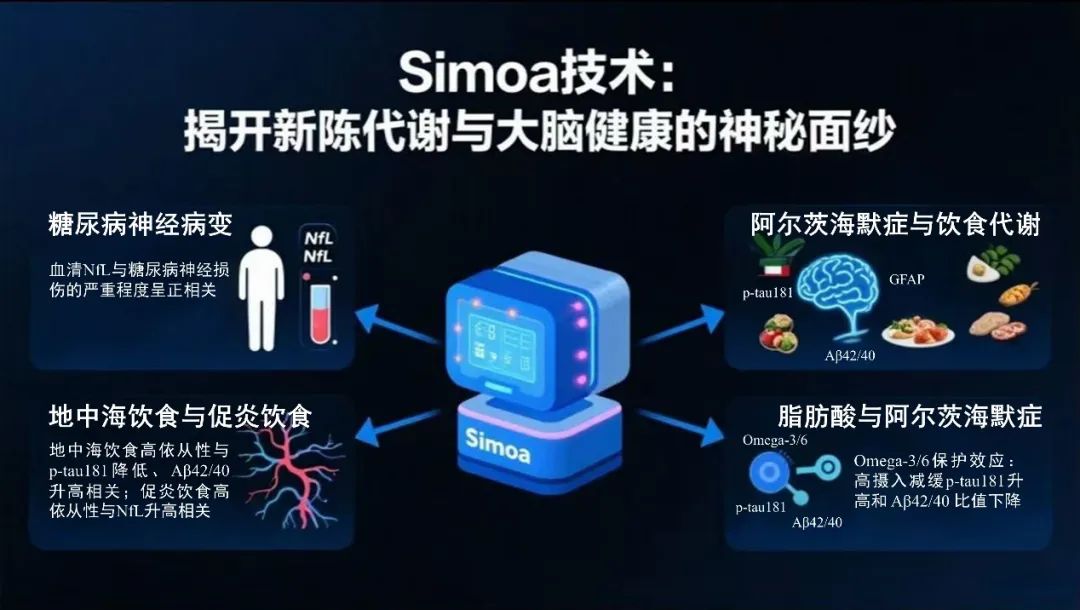
01 糖尿病代謝紊亂與神經病變:Simoa技術的精準洞察

糖尿病作為一種常見的代謝性疾病,其并發癥一直是醫學研究的重點。在糖尿病患者中,約半數會發展為糖尿病周圍神經病變(Diabetic peripheral neuropathy,DPN),這一比例令人擔憂。然而,傳統檢測方法在早期診斷和病情監測方面存在局限,難以捕捉到細微的病理變化。
Simoa技術憑借其超高的檢測靈敏度,為DPN的研究帶來了新的視角。在一項針對2型糖尿病患者的研究中,研究人員利用Simoa技術檢測血清中的神經絲輕鏈(Neurofilament light chain,NfL)水平[1]。結果發現,雖然NfL并不能作為DPN存在的可靠生物標志物,但其水平與DPN背后神經損傷的嚴重程度密切相關。具體而言,神經傳導研究(Nerve conduction study,NCS)中總和軸突NCS評分每增加1個標準差,血清NfL水平分別升高10.2%和12.1%。這一發現表明,Simoa技術能夠精準捕捉到神經損傷的細微變化,為DPN的病情評估提供了更敏感的指標。
進一步分析發現,2型糖尿病患者中,有DPN者的血清NfL水平顯著高于無DPN者(18.8ng/L vs 15.4ng/L)。這一差異在調整了年齡、性別、BMI等因素后仍然存在,充分說明了NfL與DPN神經損傷程度的相關性。Simoa技術的高靈敏度使得這種細微差異得以檢測,為臨床早期發現和干預DPN提供了可能。
02 飲食代謝模式與AD:Simoa技術揭示潛在聯系

除了糖尿病相關的神經病變,新陳代謝中的飲食模式也與大腦健康,尤其是AD的發生發展密切相關。近年來,越來越多的研究關注飲食中的脂肪酸攝入與AD生物標志物的關系,而Simoa技術在這一領域同樣發揮了重要作用。
在一項關于飲食模式與AD血液生物標志物的研究中,研究人員利用Simoa技術檢測了認知正常老年人的血漿樣本[2]。結果顯示,較高的地中海飲食(Mediterranean diet,MDS)依從性AD特異性標志物(磷酸化tau181(p-tau181)、Aβ42/40)改善相關,且在APOE-ε4攜帶者和高齡人群中更顯著。相反,更多的炎癥性飲食與更高的NfL水平相關。這一發現提示,地中海飲食可能通過調節tau蛋白的磷酸化過程,對AD的病理進程產生積極影響。

與此同時,另一項研究則聚焦于特定膳食脂肪(ω-3、ω-6和單不飽和脂肪)的攝入如何影響臨床前AD的血漿生物標志物軌跡[3]。研究發現,較高的ω-3和ω-6脂肪酸攝入與AD血液生物標志物的進展較慢相關。具體表現為,ω-3攝入較高者,其血漿中的淀粉樣蛋白β42/40比值下降較慢,p-tau181水平上升較慢;而ω-6攝入較高者,p-tau181和膠質纖維酸性蛋白(Glial fibrillary acidic protein,GFAP)的上升速度也較慢,表明可能有抗炎作用。這些結果表明,合理的脂肪酸攝入可能通過調節代謝過程,減緩AD相關的病理變化。
Simoa技術的高靈敏度和多指標檢測能力,使得研究人員能夠同時監測多種AD相關生物標志物,全面評估飲食對大腦健康的影響。例如,在檢測Aβ42/40比值、p-tau181、NfL和GFAP等指標時,Simoa技術能夠提供精準的定量數據,為深入理解飲食-代謝-大腦健康的復雜關系奠定了基礎。
03 Simoa技術:代謝與大腦健康研究的核心驅動力
Simoa技術之所以能夠在新陳代謝與大腦健康研究中發揮關鍵作用,源于其獨特的技術優勢。首先,能夠檢測到低至fg/m水平的蛋白質生物標志物,這對于捕捉早期代謝紊亂引起的細微生物標志物變化至關重要。其次,Simoa技術具備多指標檢測能力,使得研究人員能夠全面分析新陳代謝相關的多種生物標志物,如血糖、血脂、炎癥因子等。此外,Simoa技術的全自動化操作流程大大提高了檢測的重復性和準確性。這對于長期縱向研究,如追蹤代謝紊亂對大腦健康的漸進影響,具有重要意義。
> 文獻鏈接:
[1] Määttä LL, Andersen ST, Parkner T, Hviid CVB, Bjerg L, Kural MA, Charles M, Søndergaard E, Sandbæk A, Tankisi H, Witte DR, Jensen TS. Serum neurofilament light chain - A potential biomarker for polyneuropathy in type 2 diabetes? Diabetes Res Clin Pract. 2023 Nov;205:110988.
[2] Mrhar A, Carballo-Casla A, Grande G, Valletta M, Fredolini C, Fratiglioni L, Gregorič Kramberger M, Kuhar A, Winblad B, Calderón-Larrañaga A, Vetrano DL. Dietary patterns and blood-based biomarkers of Alzheimer's disease in cognitively intact older adults: Findings from a population-based study. J Prev Alzheimers Dis. 2025 Mar 14:100124.
[3] Hoost SS, Honig LS, Kang MS, Bahl A, Lee AJ, Sanchez D, Reyes-Dumeyer D, Lantigua RA, Dage JL, Brickman AM, Manly JJ, Mayeux R, Gu Y. Association of dietary fatty acids with longitudinal change in plasma-based biomarkers of Alzheimer's disease. J Prev Alzheimers Dis. 2025 May;12(5):100117.






