CytScop®系列智能細胞計數儀的核心技術創新及GMP法規下的應用場景
在生物制藥領域,從細胞與基因治療到抗體生產,細胞計數與活率分析作為貫穿整個工藝開發與生產控制的關鍵環節,其準確性與可靠性直接關系到最終產品的安全性與有效性。傳統細胞計數方法因其人為誤差大、污染風險大、標準化程度低、數據完整性弱等缺陷,難以GMP法規要求。
GMP法規升級:細胞計數面臨的新挑戰在無菌要求方面,隨著2025版GMP附錄1《無菌藥品》的實施,內容更加全面細化,對無菌藥品生產質量提出了更高標準的合規要求,凸顯了無菌保證在全生命周期中的核心地位。
在數據完整性方面,監管要求已從簡單的ALCOA原則升級到ALCOA++框架,強調數據的全面追溯與風險管控。
GMP強調從“事后檢驗”向“全過程防控”的質控轉變。這意味著每一個生產環節,包括細胞計數,都必須建立在科學、可靠且可驗證的基礎上。
為GMP而生:CytScop®的核心技術創新化繁為簡:微流控芯片重塑樣本處理
CytScop®系列智能細胞計數儀,采用專利的微流控芯片(基于低雷諾數層流、生物流體等理論,針對微尺度下細胞的流動特點與細胞生長微環境而研發設計),將臺盼藍或AOPI染料預先集成于芯片流道中。
細胞懸液注入后,即可自動完成染色、混勻過程,消除了人工配液的誤差,有效提高了計數的準確度和重復性。

CytScop®搭載的雙熒光+明場復合光學系統,明場下可清晰捕捉細胞形態細節,熒光模式下則能高效收集特異性信號,即使微小細胞也能精準成像。單次成像覆蓋更多細胞,采樣量提升顯著降低系統誤差。

CytScop®Pro 的AI模型運行時,不再需要人為設置各種參數閾值如直徑、亮度、圓度、系數等,對不同的細胞類型/生物工藝具有良好的可拓展性與更準確的泛化能力。由于AI模型通過海量真實有效的工藝數據訓練與反復測試驗證,能更加科學地識別細胞凋亡/團簇團聚等復雜細胞樣本情況。
標準化與自動化:從源頭上消除變異因子在生物制藥工藝中,標準化與自動化是確保數據可靠性和一致性的基石。CytScop® Pro智能細胞計數儀支持EAS在線自動采樣模塊集成,通過全自動工作流,從根本上消除了傳統細胞計數中的變異因子,實現在無人值守條件下連續分析細胞活率和濃度,針對需要監控的生物反應器尤為重要。
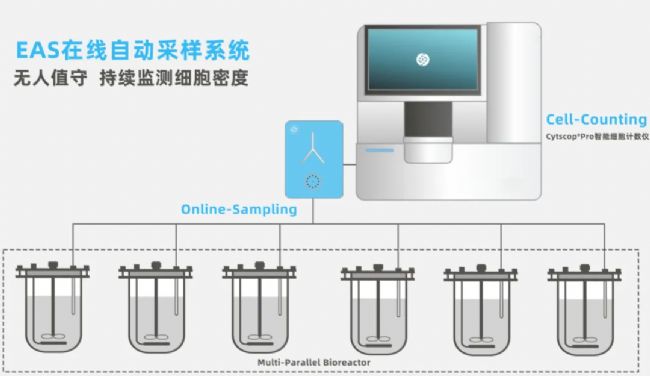
多臺儀器間的一致性驗證顯示,CytScop® Pro在不同稀釋濃度下的測量結果CV<3%,線性R²>0.999,確保了數據的可比性,為工藝轉移和放大提供了可靠基礎。
在GMP環境中,CytScop® Pro的標準化及自動化支撐了污染控制策略 的實施,通過對細胞計數過程的封閉式設計,最大限度降低了微生物污染風險。
合規與數據完整性:滿足生物制藥嚴格規范近年來,大量FDA警告信都涉及數據完整性問題,特別是缺失審計追蹤或不受控的變更。CytScop® 會自動記錄所有關鍵操作,包括用戶登錄、數據修改和結果導出等活動,確保每一個數據點的來源和處理過程都可追溯,為偏差調查和批次放行提供完整的數據支持。
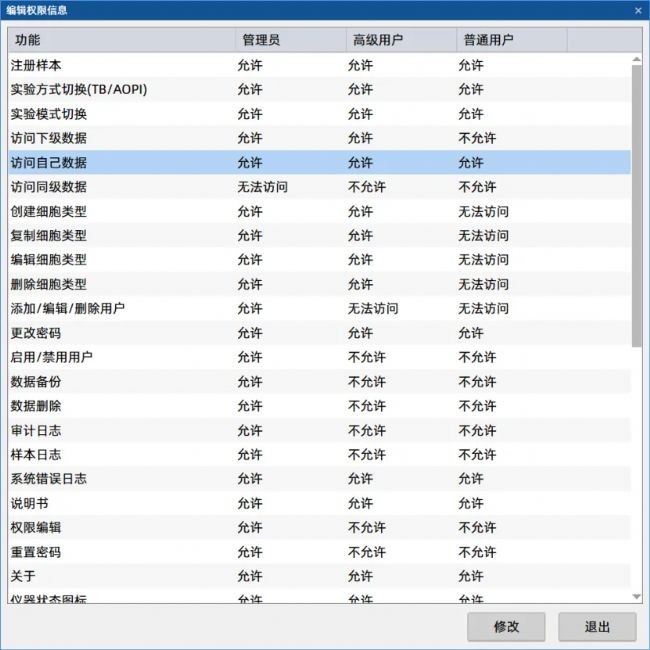
CytScop®的合規化架構不僅滿足了監管要求(FDA 21 CFR Part 11和數據完整性要求),更建立了從細胞計數到最終產品的全鏈條數據可信路徑,確保每一個基于細胞計數數據做出的工藝決策都有據可查。
應用場景全覆蓋:從研發到GMP生產CytScop®系列細胞計數儀針對生物制藥不同階段的需求,提供了從研發到GMP生產的全方位解決方案。
-
對于細胞治療產品,CytScop®的AOPI雙熒光染色能夠清晰區分活細胞、壞死細胞和凋亡細胞。這種精確的細胞狀態評估對細胞治療產品的質量與安全性至關重要。
-
在高通量工藝開發階段:CytScop® Pro能夠短時間內完成大量平行實驗的細胞分析,快速篩選最佳培養條件、培養基配方和工藝參數,其高效率特點顯著加速了工藝開發進程,同時降低了樣品消耗。
-
在GMP生產環境中,CytScop®Pro的微流控芯片避免了傳統流路污染,滿足無菌操作要求,儀器支持3Q驗證,可直接用于GMP車間的在線監控。
針對不同應用場景,浚真生命科學提供了兩款主力機型——CytScop®Pro適用于GMP車間要求高的高通量需求,而CytScop®Mini則更適合科研實驗室及細胞治療產品研發的檢測需求。

生物制藥正向著加自動化、數字化、智能化的方向邁進,正如GMP法規的持續進化,科技創新工具與質量管理體系的融合已成為行業發展的核心驅動力。從基礎的細胞計數到生物反應器放大的每一環,標準化與自動化相結合的質量控制策略,將幫助企業在激烈的市場競爭中構建起堅實的技術壁壘。






