ЗъНЧЦйҶОҝ№ХTҢ§РДјЎІЎөД°lІЎҷCЦЖөДСРҫҝ
ЗъНЧЦйҶОҝ№ЈЁTRZЈ©ЧчһйТ»·Nҝ№HER2ҶОҝЛВЎҝ№уwЈ¬лmДЬһйHER2к–РФИйПЩ°©»јХЯҺ§Ғнп@ЦшЙъҙж«@ТжЈ¬ө«•юТэ°lРДЕK¶ҫРФЈЁTICЈ©Ј¬ПЮЦЖЖдЕRҙІ‘ӘУГЈ¬ЖдҝЙҢ§ЦВРДјЎјҡ°ыҫҖБЈуw№ҰДЬХПөKЈ¬І»Я^ҫҖБЈуwЩ|БҝҝШЦЖКЗ·с…ўЕcЗъНЧЦйҶОҝ№ҪйҢ§өДРДјЎјҡ°ыҪ№НцЙРІ»Гчҙ_ЎЈ2025Дк6ФВЈ¬№ю –һIбtҝЖҙуҢW»щөAбtҢWФә—оБҰГч/АоәлСРҫҝҲFк ФЪINT J BIOL SCI (IF 10.0)ЖЪҝҜ°lұнОДХВ“Exogenous SPD inhibits trastuzumab-mediated cardiomyocyte pyroptosis through SIRT3-regulated mitochondrial quality control”Ј¬СРҫҝҪY№ыҪТКҫБЛЗъНЧЦйҶОҝ№ХTҢ§РДјЎІЎөД°lІЎҷCЦЖЈ¬ІўһйоA·АHER2+ИйПЩ°©ЦОҜҹЦРөДРДЕK¶ҫРФМṩБЛТ»ӮҖРВөДЦОҜҹ°РьcЎЈ
· ҫSХжЦъБҰ·
»щТтРЕПўЈәSIRT3Ј¬NADТАЩҮРФГ“ТТхЈГё
ІЎ¶ҫ®aЖ·ЈәAd-SIRT3
ёРИҫјҡ°ыЈәФӯҙъРЎКуРДјЎјҡ°ы
MOIЈә30
СРҫҝҪY№ы
1ЎўЗъНЧЦйҶОҝ№ХTҢ§РЎКуРДјЎҫҖБЈуwЩ|БҝҝШЦЖЧғ»Ҝ
СРҫҝҪY№ып@КҫЈ¬НвФҙРФҒҶҫ«°·МҺАнҝЙТЦЦЖTRZҪйҢ§өДРЎКуРДЕK№ҰДЬХПөKЈ¬ІўңpЙЩTRZХTҢ§өДРЎКуРДјЎјҡ°ыҪ№НцЎЈҙЛНвTRZҪoЛҺ“pәҰРЎКуРДјЎҫҖБЈуwәНРДјЎјҡ°ыҫҖБЈуwөД№ҰДЬЈ¬Ң§ЦВҫҖБЈуw“pӮыЎЈһйЯMТ»ІҪСРҫҝTRZХTҢ§РДјЎҫҖБЈуw“pӮыөДҷCЦЖЈ¬СРҫҝҲFк Фu№АБЛЖдҢҰҫҖБЈуwЩ|БҝҝШЦЖөДУ°н‘ЎЈ°l¬FTRZҪoЛҺп@ЦшҪөөНҫҖБЈуwЙъОпәПіЙПакPө°°ЧЈЁИзPGC-1αЎўNRF-1әНTFAMЈ©өДmRNAұнЯ_Ј¬ңpЙЩРДјЎҫҖБЈуwлҠЧУӮчЯfжңЦРҸНәПОпI-NDVFB8ЎўII-SDHBЎўIV-COXIVЎўV-ATP5A1өДө°°ЧШS¶ИЈ¬ҪөөНРДјЎҪMҝ—ЦРPGC-1αЎўNRF-1ЎўNRF-2әНTFAM өДө°°ЧШS¶ИЈ¬Н¬•rҢ§ЦВҫҖБЈуwИЪәПңpЙЩЎў·ЦБСФцјУЈ¬ёДЧғҫҖБЈуw„УБҰҢWЈ¬¶шНвФҙРФҒҶҫ«°·ёЙоAҝЙп@ЦшңpЭpЯ@Р©УЙTRZХTҢ§өДУ°н‘ЎЈSIRT3ЧчһйҫҖБЈуwғИөДкPжIХ{№қТтЧУЈ¬ФЪTRZМҺАнәуЈ¬ЖдФЪРЎКуРДјЎҪMҝ—ЦРөДmRNAәНө°°ЧЛ®ЖҪп@ЦшҪөөНЈ»ЕcТ°ЙъРНРЎКуПаұИЈ¬SIRT3ЗГіэРЎКуҹoХ“КЗ·сҪУКЬTRZМҺАнЈ¬уwЦШҫщп@ЦшПВҪөЈ¬ҪУКЬTRZМҺАнәуРДЕKіЯҙзёьРЎЎўРДЕKЦШБҝЕcуwЦШұИЦөп@ЦшҪөөНЈ¬РДЕK№ҰДЬп@ЦшПВҪөЈ¬ұнГчSIRT3ЗГіэФЪTRZМҺАнПВ•юјУ„ЎРДЕK“pӮыЈ¬К№РЎКуёьТЧКЬІ»АыТтЛШУ°н‘ЎЈЯMТ»ІҪСРҫҝ°l¬FSIRT3ҢҰTRZХTҢ§өДРДјЎјҡ°ыҪ№НцҫЯУРЦШТӘұЈЧoЧчУГЎЈ
· ҫSХжЦъБҰ·
»щТтРЕПўЈәSIRT3Ј¬NADТАЩҮРФГ“ТТхЈГё
ІЎ¶ҫ®aЖ·ЈәAd-SIRT3
ёРИҫјҡ°ыЈәФӯҙъРЎКуРДјЎјҡ°ы
MOIЈә30
СРҫҝҪY№ы
1ЎўЗъНЧЦйҶОҝ№ХTҢ§РЎКуРДјЎҫҖБЈуwЩ|БҝҝШЦЖЧғ»Ҝ
СРҫҝҪY№ып@КҫЈ¬НвФҙРФҒҶҫ«°·МҺАнҝЙТЦЦЖTRZҪйҢ§өДРЎКуРДЕK№ҰДЬХПөKЈ¬ІўңpЙЩTRZХTҢ§өДРЎКуРДјЎјҡ°ыҪ№НцЎЈҙЛНвTRZҪoЛҺ“pәҰРЎКуРДјЎҫҖБЈуwәНРДјЎјҡ°ыҫҖБЈуwөД№ҰДЬЈ¬Ң§ЦВҫҖБЈуw“pӮыЎЈһйЯMТ»ІҪСРҫҝTRZХTҢ§РДјЎҫҖБЈуw“pӮыөДҷCЦЖЈ¬СРҫҝҲFк Фu№АБЛЖдҢҰҫҖБЈуwЩ|БҝҝШЦЖөДУ°н‘ЎЈ°l¬FTRZҪoЛҺп@ЦшҪөөНҫҖБЈуwЙъОпәПіЙПакPө°°ЧЈЁИзPGC-1αЎўNRF-1әНTFAMЈ©өДmRNAұнЯ_Ј¬ңpЙЩРДјЎҫҖБЈуwлҠЧУӮчЯfжңЦРҸНәПОпI-NDVFB8ЎўII-SDHBЎўIV-COXIVЎўV-ATP5A1өДө°°ЧШS¶ИЈ¬ҪөөНРДјЎҪMҝ—ЦРPGC-1αЎўNRF-1ЎўNRF-2әНTFAM өДө°°ЧШS¶ИЈ¬Н¬•rҢ§ЦВҫҖБЈуwИЪәПңpЙЩЎў·ЦБСФцјУЈ¬ёДЧғҫҖБЈуw„УБҰҢWЈ¬¶шНвФҙРФҒҶҫ«°·ёЙоAҝЙп@ЦшңpЭpЯ@Р©УЙTRZХTҢ§өДУ°н‘ЎЈSIRT3ЧчһйҫҖБЈуwғИөДкPжIХ{№қТтЧУЈ¬ФЪTRZМҺАнәуЈ¬ЖдФЪРЎКуРДјЎҪMҝ—ЦРөДmRNAәНө°°ЧЛ®ЖҪп@ЦшҪөөНЈ»ЕcТ°ЙъРНРЎКуПаұИЈ¬SIRT3ЗГіэРЎКуҹoХ“КЗ·сҪУКЬTRZМҺАнЈ¬уwЦШҫщп@ЦшПВҪөЈ¬ҪУКЬTRZМҺАнәуРДЕKіЯҙзёьРЎЎўРДЕKЦШБҝЕcуwЦШұИЦөп@ЦшҪөөНЈ¬РДЕK№ҰДЬп@ЦшПВҪөЈ¬ұнГчSIRT3ЗГіэФЪTRZМҺАнПВ•юјУ„ЎРДЕK“pӮыЈ¬К№РЎКуёьТЧКЬІ»АыТтЛШУ°н‘ЎЈЯMТ»ІҪСРҫҝ°l¬FSIRT3ҢҰTRZХTҢ§өДРДјЎјҡ°ыҪ№НцҫЯУРЦШТӘұЈЧoЧчУГЎЈ
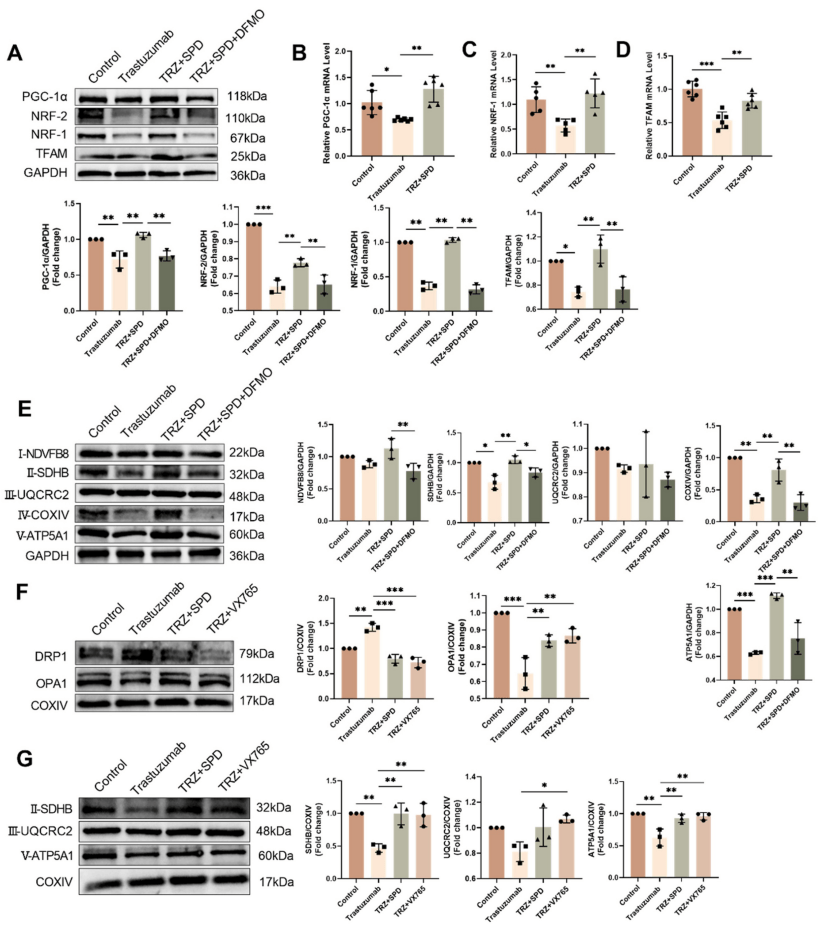
ЗъНЧЦйҶОҝ№ҢҰҫҖБЈуwө°°ЧұнЯ_өДУ°н‘
2ЎўSIRT3ФЪTRZҪйҢ§өДСх»Ҝ‘ӘјӨЦРЖрұЈЧoЧчУГ
GOё»јҜ·ЦОцп@Кҫ SIRT3-KOРЎКуЕcWTРЎКуөД»щТт№ҰДЬІо®җЙжј°ҫҖБЈуwәфОьжңҸНәПуw2ЙъОп°lЙъЎўСх»ҜЯҖФӯГё»оРФХэХ{ҝШөИЯ^іМЈ»ЯMТ»ІҪСРҫҝЧCГчTRZМҺАнјҡ°ыЦРAMPK-PGC-1a-Sirt3НЁВ·ҢҰҫҖБЈуwЖрұЈЧoЧчУГЎЈKEGGё»јҜ·ЦОцп@Кҫ SIRT3-KOРЎКуЕcWTРЎКуөД»щТт№ҰДЬІо®җЕcСх»Ҝ‘ӘјӨп@ЦшПакPЈ»TRZМҺАнК№ WTРЎКуРДјЎҪMҝ—ЦРCATө°°ЧШS¶Ип@ЦшҪөөНЈ¬SIRT3-KOРЎКуTRZҪMCATө°°ЧұнЯ_Э^WTРЎКуTRZҪMЯMТ»ІҪп@ЦшҪөөНЈ»ФЪФӯҙъіЙАwҫSјҡ°ыЦРЈ¬јҡ°ы»оРФСхЗеіэ„©NACҝЙТЦЦЖTRZХTҢ§өДCOL1ЎўCOL3әНα-SMAұнЯ_ЙПХ{Ј»HL-1јҡ°ыЦРЈ¬SIRT3Я^ұнЯ_ҝЙЧиөKTRZҪйҢ§өДCATұнЯ_ҪөөНЈ»ҫҖБЈуw»оРФСхЗеіэ„© Mito-TempoЕcNACҪY№ыТ»ЦВЈ¬ҫщДЬТЦЦЖTRZҪйҢ§өДіЙАwҫSјҡ°ыАwҫS»ҜФцҸҠЈ¬ЗТNACМҺАнҝЙјУ„ЎTRZҪйҢ§өДіЙАwҫSјҡ°ыДӨлҠО»ҪөөНЈ¬ұнГчТЦЦЖСх»Ҝ‘ӘјӨҝЙңpЭpTRZХTҢ§өДіЙАwҫSјҡ°ыАwҫS»ҜЎЈ
GOё»јҜ·ЦОцп@Кҫ SIRT3-KOРЎКуЕcWTРЎКуөД»щТт№ҰДЬІо®җЙжј°ҫҖБЈуwәфОьжңҸНәПуw2ЙъОп°lЙъЎўСх»ҜЯҖФӯГё»оРФХэХ{ҝШөИЯ^іМЈ»ЯMТ»ІҪСРҫҝЧCГчTRZМҺАнјҡ°ыЦРAMPK-PGC-1a-Sirt3НЁВ·ҢҰҫҖБЈуwЖрұЈЧoЧчУГЎЈKEGGё»јҜ·ЦОцп@Кҫ SIRT3-KOРЎКуЕcWTРЎКуөД»щТт№ҰДЬІо®җЕcСх»Ҝ‘ӘјӨп@ЦшПакPЈ»TRZМҺАнК№ WTРЎКуРДјЎҪMҝ—ЦРCATө°°ЧШS¶Ип@ЦшҪөөНЈ¬SIRT3-KOРЎКуTRZҪMCATө°°ЧұнЯ_Э^WTРЎКуTRZҪMЯMТ»ІҪп@ЦшҪөөНЈ»ФЪФӯҙъіЙАwҫSјҡ°ыЦРЈ¬јҡ°ы»оРФСхЗеіэ„©NACҝЙТЦЦЖTRZХTҢ§өДCOL1ЎўCOL3әНα-SMAұнЯ_ЙПХ{Ј»HL-1јҡ°ыЦРЈ¬SIRT3Я^ұнЯ_ҝЙЧиөKTRZҪйҢ§өДCATұнЯ_ҪөөНЈ»ҫҖБЈуw»оРФСхЗеіэ„© Mito-TempoЕcNACҪY№ыТ»ЦВЈ¬ҫщДЬТЦЦЖTRZҪйҢ§өДіЙАwҫSјҡ°ыАwҫS»ҜФцҸҠЈ¬ЗТNACМҺАнҝЙјУ„ЎTRZҪйҢ§өДіЙАwҫSјҡ°ыДӨлҠО»ҪөөНЈ¬ұнГчТЦЦЖСх»Ҝ‘ӘјӨҝЙңpЭpTRZХTҢ§өДіЙАwҫSјҡ°ыАwҫS»ҜЎЈ
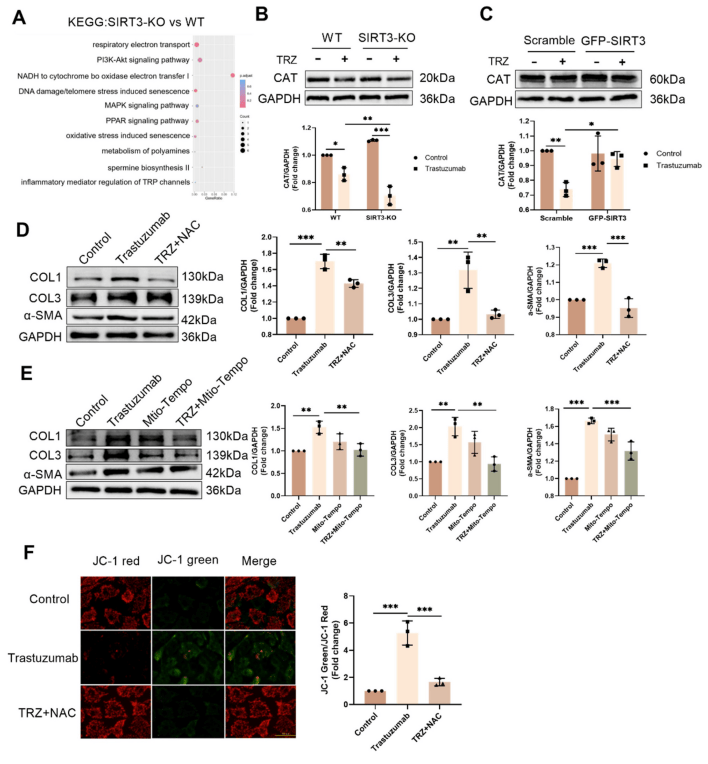
SIRT3ФЪTRZҪйҢ§өДСх»Ҝ‘ӘјӨЦРЖрұЈЧoЧчУГ
3ЎўНвФҙРФҒҶҫ«°·НЁЯ^SIRT3ұЈЧoTRZХTҢ§өДРДјЎ“pӮы
GOё»јҜ·ЦОцп@КҫSIRT3-KO+TRZҪMЕcWT+TRZҪMөД»щТт№ҰДЬІо®җЙжј°ҫҖБЈуwғИДӨәНДzФӯ·ЦҪвҙъЦxЈ¬ЯMТ»ІҪөД·ЦОцұнГчЗъНЧЦйҶОҝ№ТЦЦЖPI3 K/AKTНЁВ·БЧЛб»ҜЈ¬ЖЖүДҫҖБЈуw„УБҰҢWЈ¬ТЦЦЖҫҖБЈуwИЪәПЈ¬ҙЩЯMҫҖБЈуw·ЦБСЈ¬ІўТтҙЛҢ§ЦВФцҸҠөДАwҫS»ҜЎЈФЪSIRT3»щТтЗГіэРЎКуөДTRZХTҢ§РДЕK¶ҫРФ“pӮыДЈРНЦРМнјУНвФҙРФҒҶҫ«°·ёЙоAәуЈ¬СРҫҝҲFк ЯMТ»ІҪМҪҫҝБЛSIRT3КЗ·сКЗНвФҙРФҒҶҫ«°·ұЈЧoTRZХTҢ§өДРДјЎ¶ҫРФөДЦШТӘТтЛШЎЈҪY№ып@КҫЈ¬НвФҙРФҒҶҫ«°·өДЧчУГФЪSIRT3-KOРЎКуЦРңpИхЙхЦБПыК§Ј¬ХfГчНвФҙРФҒҶҫ«°·НЁЯ^SIRT3ҙЩЯMҫҖБЈуwЙъОпәПіЙЈ¬ёДЙЖTRZХTҢ§өДСх»Ҝ‘ӘјӨәНРДјЎјҡ°ыөтНцЎЈ
GOё»јҜ·ЦОцп@КҫSIRT3-KO+TRZҪMЕcWT+TRZҪMөД»щТт№ҰДЬІо®җЙжј°ҫҖБЈуwғИДӨәНДzФӯ·ЦҪвҙъЦxЈ¬ЯMТ»ІҪөД·ЦОцұнГчЗъНЧЦйҶОҝ№ТЦЦЖPI3 K/AKTНЁВ·БЧЛб»ҜЈ¬ЖЖүДҫҖБЈуw„УБҰҢWЈ¬ТЦЦЖҫҖБЈуwИЪәПЈ¬ҙЩЯMҫҖБЈуw·ЦБСЈ¬ІўТтҙЛҢ§ЦВФцҸҠөДАwҫS»ҜЎЈФЪSIRT3»щТтЗГіэРЎКуөДTRZХTҢ§РДЕK¶ҫРФ“pӮыДЈРНЦРМнјУНвФҙРФҒҶҫ«°·ёЙоAәуЈ¬СРҫҝҲFк ЯMТ»ІҪМҪҫҝБЛSIRT3КЗ·сКЗНвФҙРФҒҶҫ«°·ұЈЧoTRZХTҢ§өДРДјЎ¶ҫРФөДЦШТӘТтЛШЎЈҪY№ып@КҫЈ¬НвФҙРФҒҶҫ«°·өДЧчУГФЪSIRT3-KOРЎКуЦРңpИхЙхЦБПыК§Ј¬ХfГчНвФҙРФҒҶҫ«°·НЁЯ^SIRT3ҙЩЯMҫҖБЈуwЙъОпәПіЙЈ¬ёДЙЖTRZХTҢ§өДСх»Ҝ‘ӘјӨәНРДјЎјҡ°ыөтНцЎЈ
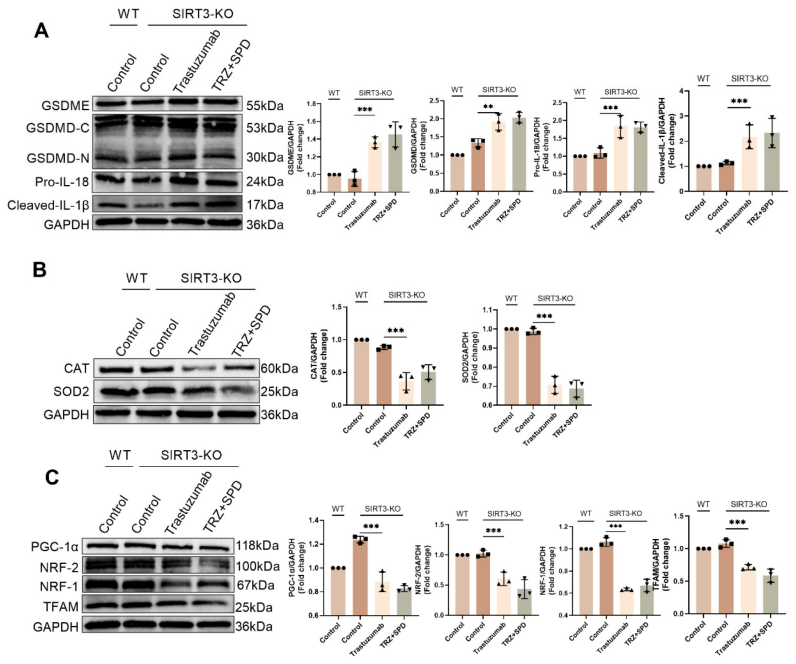
НвФҙРФҒҶҫ«°·НЁЯ^SIRT3ұЈЧoЗъНЧЦйҶОҝ№“pӮыРДјЎҪMҝ—
СРҫҝҪYХ“
ұҫСРҫҝ°l¬FЗъНЧЦйҶОҝ№ЈЁTRZЈ©ХTҢ§РДјЎјҡ°ыөтНцІў“pәҰРДЕK№ҰДЬЈ¬МШ„eКЗФЪSIRT3»щТтЗГіэРЎКуЦРЈ¬јУ„ЎБЛTRZХTҢ§өД“pӮыіМ¶ИЎЈҙЛНвНвФҙРФҒҶҫ«°·ҝЙңpЭpTRZҪйҢ§өДРДЕK“pӮыЈ¬І»ғHһйTRZРДЕK¶ҫРФөДЦОҜҹМṩБЛТ»ӮҖқ“ФЪөДРВ°РьcЈ¬ТІһйTRZҪйҢ§өДД[БцРДЕKЦОҜҹөДЕRҙІ‘ӘУГөм¶ЁБЛҢҚтһ»щөAЎЈ
ұҫСРҫҝ°l¬FЗъНЧЦйҶОҝ№ЈЁTRZЈ©ХTҢ§РДјЎјҡ°ыөтНцІў“pәҰРДЕK№ҰДЬЈ¬МШ„eКЗФЪSIRT3»щТтЗГіэРЎКуЦРЈ¬јУ„ЎБЛTRZХTҢ§өД“pӮыіМ¶ИЎЈҙЛНвНвФҙРФҒҶҫ«°·ҝЙңpЭpTRZҪйҢ§өДРДЕK“pӮыЈ¬І»ғHһйTRZРДЕK¶ҫРФөДЦОҜҹМṩБЛТ»ӮҖқ“ФЪөДРВ°РьcЈ¬ТІһйTRZҪйҢ§өДД[БцРДЕKЦОҜҹөДЕRҙІ‘ӘУГөм¶ЁБЛҢҚтһ»щөAЎЈ
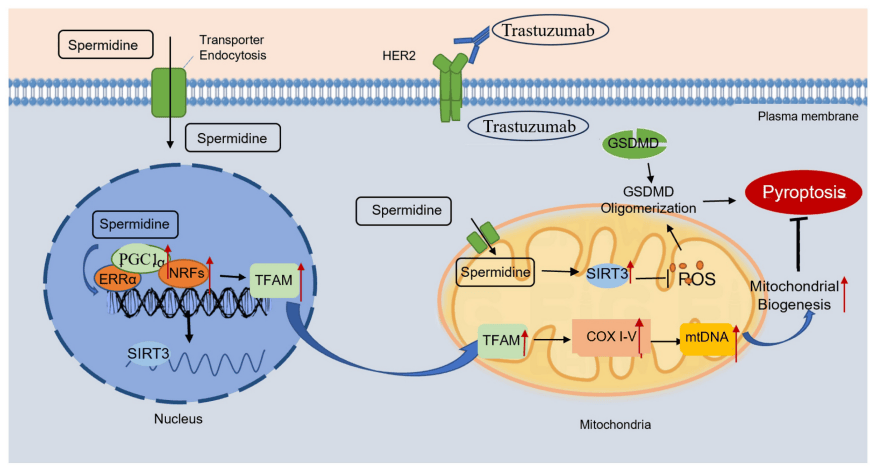
- ФцҸҠAAVҢҰДIЕKҪMҝ—өДёРИҫР§ВКөД·Ҫ·Ё·ЦПн
- ОД«IЈәAAAЦРғИЖӨјҡ°ыФЪҶОјҡ°ыЛ®ЖҪЙПөД®җЩ|РФәНЮDдӣМШХч
- аҸО»ЯBҪУјјРg(PLA)өДФӯАнЎўҢҚтһБчіМј°ФЪЙъГьҝЖҢWСРҫҝЦРөД‘ӘУГ
- ЛҘАПҳЛЦҫөДТт№ыкPПөЈә¶ЛБЈ/rDNAІЕКЗёщұҫТтЛШЈҝ
- ө°°ЧЩ|ҪYҳӢоAңyөДјјРgЧғёпЎўРВМф‘рЕc°lХ№·ҪПт
- ҝХйg¶аҪMҢWЦъБҰҪТКҫДzЩ|БцЦРИэјүБЬ°НҪYҳӢөДЕRҙІТвБx
- CZ CELLxGENE DiscoverЙъОп”ө“юҺмК№УГІҪуEҪйҪB
- CosMx SMIҝХйgФӯО»јјРgЦъБҰҹoРиҪMҝ—ҪвлxҢҚ¬FҶОјҡ°ыөД¶а°РҳЛҷzңy
- ЙПәЈЙъОпРҫЖ¬НЖіцSMI WTXЕcҝХйgө°°ЧВ“әПҷzңy·Ҫ°ё
- ҳ·ӮдҢҚө°°ЧҷzңyЖҙ°еЎўЪ…»ҜТтЧУҷzңy¶аЦШДкҪKёЈАый_Ҷў
- ЙПәЈЙъОпРҫЖ¬јҙҢўНЖіц"СӘ№Ь»ҜЖч№ЩРҫЖ¬"®aЖ·әН·ю„Х
- ЙъОпРҫЖ¬НЖіцWTXЕc¶аЖҪЕ_ө°°ЧҪMҷzңyјјРgҪвӣQ·Ҫ°ё
- ҳ·ӮдҢҚИ«ҫҖ·ю„Х®aЖ·ҙуҙЩЈ¬қMңpҒнТuЈ¬Жҙ°еқM10ЛН1
- ҮшғИКЧЕъCosMx SMI WTXёЯНЁБҝЮDдӣҪMҢҚңy”ө“юіц t
- Bruker°lІјGeoMx® DPAЈ¬ҢҚ¬F1200+·Nө°°ЧЩ|ҝХйgұнЯ_
- SBCРҫҝХТ»М–®aЖ·ЦРөДкPжIјјРgЖҪЕ_SMIНкіЙЦШҙуЙэјү
Copyright(C) 1998-2025 ЙъОпЖчІДҫW лҠФ’Јә021-64166852;13621656896 E-mailЈәinfo@bio-equip.com






