基因編輯技術TALEN的組成、作用原理及應用范圍
與 ZFN 類似,TALEN 也由兩部分組成:N 端—來自植物病原體黃單胞菌屬的轉錄激活因子樣效應物(TALE)DNA 結合域,C 端—FokI 限制性內切酶催化域。TALE 蛋白由大約 34 個氨基酸組成,第 12和 13 位氨基酸被稱為重復可變的雙氨基酸殘基(repeat variable di-residue,RVD),決定了 TALE 識別并結合的 DNA 序列,除 12 和 13 位外的其余氨基酸都是保守的。此外,TALEN 也以二聚體形式發揮作用,分別靶向不同的 DNA 鏈。TALEN 的靶向目標序列長度通常為 30 ~ 40 bp。
TALEN 相對于 ZFN 的優勢在于它們可以識別單個核苷酸,只需要設計 1 個 TALE 分子就可以識別一個堿基,理論上可以靶向基因組任何區域,不過工作量相對變大;此外,TALEN 在人類細胞中的細胞毒性較低。該系統已被證明能有效地在體細胞和多能干細胞中引入 DSBs。
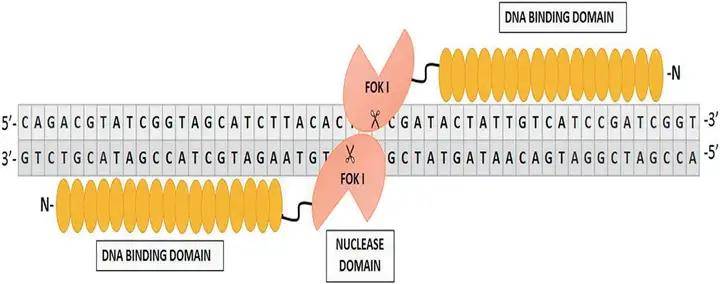
TALEN 結構示意圖
TALEN 優點
- 高特異性:TALE 結構域識別的 DNA 序列較長(通常 16-20 個堿基),脫靶效應較低(相比早期的鋅指核酸酶 ZFN 更穩定)。
- 普適性:理論上可靶向任意 DNA 序列(僅受 RVD 與堿基對應關系限制),適用范圍廣。
- 構建復雜:TALE 重復單元的克隆和組裝過程繁瑣(需拼接多個重復序列),耗時且成本較高。
- 蛋白較大:TALEN 復合體分子量較大,通過病毒載體遞送時效率較低(相比 CRISPR 的 Cas9 蛋白更難進入細胞)。
隨著 CRISPR 技術的普及,TALEN 的應用范圍有所縮小,但研究者通過優化其構建方法(如自動化組裝平臺)和遞送系統(如脂質納米顆粒),仍在推動其發展。目前,TALEN 在一些對脫靶效應要求嚴苛的領域(如基因治療)仍被視為重要備選工具,其高特異性的特點使其在精準編輯中具有不可替代的優勢。
總之,TALEN 作為基因編輯技術發展中的重要里程碑,不僅推動了早期基因編輯的實用化,也為后續技術(如 CRISPR)的優化提供了參考,至今仍在特定領域發揮著重要作用。
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






