人骨髓間充質基質細胞MSC微流體高通量單細胞封裝技術的介紹
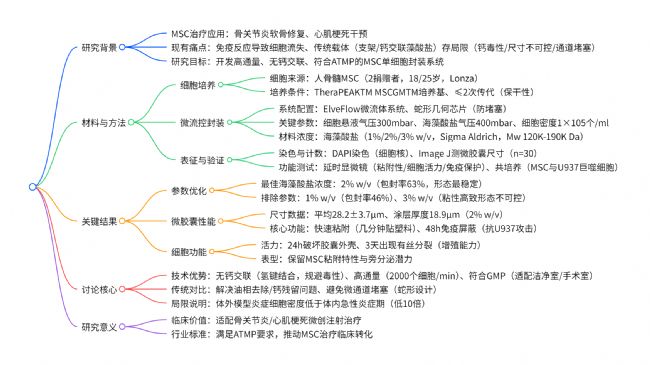
該研究針對干細胞治療中人骨髓間充質基質細胞(MSC) 移植需逃避早期免疫反應、保留在移植部位的核心需求,開發了新型微流體高通量單細胞封裝系統;該系統以2% w/v 海藻酸鹽為封裝材料,通過海藻酸鹽羥基與細胞糖萼形成氫鍵實現無鈣交聯,規避傳統鈣交聯的細胞毒性與尺寸不可控問題,最終實現2000 個細胞 /min 的最佳單細胞包封率,微膠囊平均尺寸達28.2±3.7µm且形態可復制;實驗驗證顯示,封裝細胞可快速粘附組織培養塑料,24h 后能破壞微膠囊外殼并增殖,3 天出現有絲分裂,且在與不同密度 U937 巨噬細胞共培養 48h 內保持結構完整,為符合高級治療藥物產品(ATMP)標準的 MSC 微創治療(骨關節炎、心肌梗死)奠定基礎。
移植后易受早期免疫反應攻擊(如關節內腫脹、下背痛,7 天緩解);
傳統載體局限:組織工程支架不適配微創注射,鈣交聯藻酸鹽微珠存在鈣毒性、尺寸不可控及油相 / 未反應鈣去除耗時(危害細胞活力)。
研究目標:開發一種高通量、可重復、無鈣交聯的微流體 MSC 單細胞封裝系統,滿足微創移植需求,同時保障細胞粘附性、活力與免疫保護。
二、材料與方法
2.1 細胞培養
2.2 微流控封裝系統
核心設備:ElveFlow 微流體系統(法國),含壓力控制器、蛇形幾何芯片(延長通道防細胞聚集)、DG-DM-60/1.2 mm 液滴發生器;
消毒流程:所有組件(管道、芯片)用 70% v/v 乙醇 / 水消毒 1h,入口處 0.2μm 過濾器過濾;
關鍵操作參數:
氣壓:細胞懸液通道300mbar(防聚集),海藻酸鹽通道400mbar;
海藻酸鹽濃度:測試 1%、2%、3% w/v(Sigma Aldrich,Mw 120K-190K Da);
收集與孵育:封裝后收集于無菌 Eppendorf 管,懸浮 30min 后用于實驗。
2.3 表征與功能驗證
形態與尺寸:DAPI 染色(細胞核可視化),Image J 軟件測量 30 個微膠囊直徑(校準像素為微米);
粘附與活力:2×105 個細胞 /ml 接種于組織培養塑料,37℃、5% CO2 孵育 3 天,Axion 無線顯微鏡觀察;
免疫保護:與 U937 單核細胞 / 巨噬細胞(密度 2×105~5×105 個 /ml)共培養 2 天,延時顯微鏡監測微膠囊完整性。
三、關鍵實驗結果
3.1 系統參數優化
3.2 微膠囊尺寸與涂層厚度
2% w/v 海藻酸鹽封裝的 MSC:平均尺寸28.2±3.7µm,涂層厚度間接估計為18.9µm;
未封裝 MSC:平均尺寸 9.3±1.8µm;
1% w/v 海藻酸鹽封裝:涂層厚度僅 5µm(免疫保護與粘附潛力不足)。
3.3 粘附與細胞增殖能力
粘附性:封裝細胞幾分鐘內沉積于孔底,未封裝細胞漂浮數小時;
增殖活力:24h 后封裝細胞開始破壞微膠囊外殼,3 天觀察到有絲分裂跡象(黑色箭頭,圖 5),證明保留增殖能力。
3.4 免疫保護效果
共培養實驗:U937 巨噬細胞在 7~8h 開始攻擊封裝 MSC,24h 形成密集包圍簇;
保護結果:無論 U937 接種密度如何,封裝 MSC 在48h 內保持結構完整,驗證早期免疫屏蔽作用。

一、研究背景與目標
干細胞治療中,人骨髓間充質基質細胞(MSC) 因多向分化(脂肪細胞 / 軟骨細胞 / 成骨細胞)、旁分泌調節(如 VEGF)及抗炎特性,被用于骨關節炎軟骨修復(23 項非案例研究,13 項隨機對照)與心肌梗死干預,但存在兩大核心問題:移植后易受早期免疫反應攻擊(如關節內腫脹、下背痛,7 天緩解);
傳統載體局限:組織工程支架不適配微創注射,鈣交聯藻酸鹽微珠存在鈣毒性、尺寸不可控及油相 / 未反應鈣去除耗時(危害細胞活力)。
研究目標:開發一種高通量、可重復、無鈣交聯的微流體 MSC 單細胞封裝系統,滿足微創移植需求,同時保障細胞粘附性、活力與免疫保護。
二、材料與方法
2.1 細胞培養
| 項目 | 具體參數 |
| 細胞來源 | 人骨髓 MSC(2 名捐贈者:男性 18 歲、女性 25 歲,英國 Lonza) |
| 培養基 | 化學定義培養基(Lonza TheraPEAKTM MSCGMTM,無血清) |
| 傳代要求 | 封裝前≤2 次傳代(維持 MSC 干性) |
| 細胞懸液密度 | 測試范圍 1×105~1×106 個 /ml,最終優化為1×105 個 /ml(避免通道堵塞) |
2.2 微流控封裝系統
核心設備:ElveFlow 微流體系統(法國),含壓力控制器、蛇形幾何芯片(延長通道防細胞聚集)、DG-DM-60/1.2 mm 液滴發生器;
消毒流程:所有組件(管道、芯片)用 70% v/v 乙醇 / 水消毒 1h,入口處 0.2μm 過濾器過濾;
關鍵操作參數:
氣壓:細胞懸液通道300mbar(防聚集),海藻酸鹽通道400mbar;
海藻酸鹽濃度:測試 1%、2%、3% w/v(Sigma Aldrich,Mw 120K-190K Da);
收集與孵育:封裝后收集于無菌 Eppendorf 管,懸浮 30min 后用于實驗。
2.3 表征與功能驗證
形態與尺寸:DAPI 染色(細胞核可視化),Image J 軟件測量 30 個微膠囊直徑(校準像素為微米);
粘附與活力:2×105 個細胞 /ml 接種于組織培養塑料,37℃、5% CO2 孵育 3 天,Axion 無線顯微鏡觀察;
免疫保護:與 U937 單核細胞 / 巨噬細胞(密度 2×105~5×105 個 /ml)共培養 2 天,延時顯微鏡監測微膠囊完整性。
三、關鍵實驗結果
3.1 系統參數優化
| 優化指標 | 測試條件 | 最佳參數 | 關鍵結果 |
| 細胞密度 | 1×105~1×106 個 /ml | 1×105 個 /ml | 密度過高(1×106 個 /ml)導致芯片儲庫 / 中央通道堵塞(圖 2) |
| 海藻酸鹽濃度 | 1%/2%/3% w/v | 2% w/v | 1% 包封率 46%,2% 包封率63% 且形態可復制,3% 粘性過高致形態不可控 |
| 氣壓參數 | 細胞 200~400mbar,海藻酸鹽 300~500mbar | 細胞 300mbar,海藻酸鹽 400mbar | 該組合實現單細胞穩定注入,無聚集或通道堵塞 |
3.2 微膠囊尺寸與涂層厚度
2% w/v 海藻酸鹽封裝的 MSC:平均尺寸28.2±3.7µm,涂層厚度間接估計為18.9µm;
未封裝 MSC:平均尺寸 9.3±1.8µm;
1% w/v 海藻酸鹽封裝:涂層厚度僅 5µm(免疫保護與粘附潛力不足)。
3.3 粘附與細胞增殖能力
粘附性:封裝細胞幾分鐘內沉積于孔底,未封裝細胞漂浮數小時;
增殖活力:24h 后封裝細胞開始破壞微膠囊外殼,3 天觀察到有絲分裂跡象(黑色箭頭,圖 5),證明保留增殖能力。
3.4 免疫保護效果
共培養實驗:U937 巨噬細胞在 7~8h 開始攻擊封裝 MSC,24h 形成密集包圍簇;
保護結果:無論 U937 接種密度如何,封裝 MSC 在48h 內保持結構完整,驗證早期免疫屏蔽作用。
3.4. 討論與分析
技術突破:通過海藻酸鹽羥基與細胞糖萼形成直接氫鍵,首次實現無鈣交聯的 MSC 單細胞封裝,規避傳統鈣交聯的毒性與油相去除問題;
優勢對比:蛇形芯片設計減少壓降與堵塞,2000 個細胞 /min 的高通量遠超傳統方法,且微膠囊尺寸適配微創注射;
臨床適配性:藻酸鹽獲 FDA 批準用于醫療,系統符合GMP 規范,可容納于潔凈室或手術室,適配骨關節炎(關節內注射)與心肌梗死(局部注射)場景;
局限性:體外模型中 U937 密度(2×105~5×105 個 /ml)低于體內炎性關節病急性期(5×104 個 /ml,低 10 倍),需后續體內實驗驗證。
3.5. 研究總結與意義
本研究成功開發了微流體高通量 MSC 單細胞封裝系統,核心成果包括:
確定 2% w/v 海藻酸鹽、1×105 個 /ml 細胞密度等最優參數,實現 63% 包封率與 28.2±3.7µm 的可控微膠囊尺寸;
驗證封裝細胞保留粘附、增殖能力,且微膠囊提供 48h 免疫保護;
系統符合 ATMP 標準,為 MSC 微創治療(骨關節炎、心肌梗死)提供可規模化、規范化的制造方案,推動干細胞治療從臨床前向臨床轉化。
四、關鍵問題與答案
問題 1:該研究開發的微流體 MSC 封裝系統,相比傳統藻酸鹽封裝技術,核心技術創新點是什么?
答案:核心創新在于無鈣交聯機制與高通量可控性:
摒棄傳統藻酸鹽 - 鈣離子交聯(避免鈣毒性與尺寸不可控),通過海藻酸鹽羥基與細胞糖萼形成直接氫鍵實現穩定涂層;
采用蛇形幾何微流控芯片與精準氣壓控制(細胞 300mbar、海藻酸鹽 400mbar),解決傳統微流體通道堵塞問題,實現2000 個細胞 /min 的高通量封裝;
微膠囊尺寸精準可控(28.2±3.7µm),且無需后續油相或未反應鈣去除步驟,縮短流程并保障細胞活力(24h 破殼增殖,3 天有絲分裂)。
問題 2:研究通過哪些實驗驗證了 “封裝 MSC 滿足臨床移植需求” 這一核心假設?具體結果如何?
答案:通過三大功能驗證實驗,證明封裝 MSC 的臨床適配性:
粘附性驗證:2×105 個細胞 /ml 接種于組織培養塑料,封裝細胞幾分鐘內沉積孔底,未封裝細胞漂浮數小時,證明其可快速保留在移植部位;
活力與增殖驗證:延時顯微鏡觀察顯示,封裝 MSC 在24h 后逐漸破壞微膠囊外殼,3 天出現有絲分裂跡象,證明其保留增殖能力(核心治療功能);
免疫保護驗證:與 2×105~5×105 個 /ml 的 U937 巨噬細胞共培養 48h,盡管巨噬細胞 7~8h 開始攻擊并形成包圍簇,但封裝 MSC 始終保持結構完整,證明其可抵御早期免疫反應。
問題 3:該微流體封裝系統在臨床轉化中,相比現有 MSC 治療方案(如直接注射、支架載體),具備哪些獨特的臨床優勢?
答案:具備三大臨床優勢,適配微創治療場景:
微創兼容性:微膠囊尺寸 28.2±3.7µm,可通過內窺鏡或局部注射給藥,規避傳統組織工程支架需外科植入的問題,適配骨關節炎(關節內注射)與心肌梗死(局部注射);
制造規范性:系統符合GMP 標準,組件可消毒且體積緊湊,可容納于潔凈室或手術室,解決現有方案制造流程不可控(如細胞劑量異質性)的問題;
材料安全性:采用 FDA 批準的藻酸鹽材料,無鈣交聯避免毒性,且微膠囊涂層厚度 18.9µm(1% 濃度僅 5µm),既保障免疫保護(48h 屏蔽巨噬細胞),又不影響細胞后續增殖與功能發揮(24h 破殼)。
關注我們了解更多內容
ELVEFLOW認證的中國授權經銷商:
上海跡亞國際商貿有限公司
Gaia China Co.,Ltd.
技術突破:通過海藻酸鹽羥基與細胞糖萼形成直接氫鍵,首次實現無鈣交聯的 MSC 單細胞封裝,規避傳統鈣交聯的毒性與油相去除問題;
優勢對比:蛇形芯片設計減少壓降與堵塞,2000 個細胞 /min 的高通量遠超傳統方法,且微膠囊尺寸適配微創注射;
臨床適配性:藻酸鹽獲 FDA 批準用于醫療,系統符合GMP 規范,可容納于潔凈室或手術室,適配骨關節炎(關節內注射)與心肌梗死(局部注射)場景;
局限性:體外模型中 U937 密度(2×105~5×105 個 /ml)低于體內炎性關節病急性期(5×104 個 /ml,低 10 倍),需后續體內實驗驗證。
3.5. 研究總結與意義
本研究成功開發了微流體高通量 MSC 單細胞封裝系統,核心成果包括:
確定 2% w/v 海藻酸鹽、1×105 個 /ml 細胞密度等最優參數,實現 63% 包封率與 28.2±3.7µm 的可控微膠囊尺寸;
驗證封裝細胞保留粘附、增殖能力,且微膠囊提供 48h 免疫保護;
系統符合 ATMP 標準,為 MSC 微創治療(骨關節炎、心肌梗死)提供可規模化、規范化的制造方案,推動干細胞治療從臨床前向臨床轉化。
四、關鍵問題與答案
問題 1:該研究開發的微流體 MSC 封裝系統,相比傳統藻酸鹽封裝技術,核心技術創新點是什么?
答案:核心創新在于無鈣交聯機制與高通量可控性:
摒棄傳統藻酸鹽 - 鈣離子交聯(避免鈣毒性與尺寸不可控),通過海藻酸鹽羥基與細胞糖萼形成直接氫鍵實現穩定涂層;
采用蛇形幾何微流控芯片與精準氣壓控制(細胞 300mbar、海藻酸鹽 400mbar),解決傳統微流體通道堵塞問題,實現2000 個細胞 /min 的高通量封裝;
微膠囊尺寸精準可控(28.2±3.7µm),且無需后續油相或未反應鈣去除步驟,縮短流程并保障細胞活力(24h 破殼增殖,3 天有絲分裂)。
問題 2:研究通過哪些實驗驗證了 “封裝 MSC 滿足臨床移植需求” 這一核心假設?具體結果如何?
答案:通過三大功能驗證實驗,證明封裝 MSC 的臨床適配性:
粘附性驗證:2×105 個細胞 /ml 接種于組織培養塑料,封裝細胞幾分鐘內沉積孔底,未封裝細胞漂浮數小時,證明其可快速保留在移植部位;
活力與增殖驗證:延時顯微鏡觀察顯示,封裝 MSC 在24h 后逐漸破壞微膠囊外殼,3 天出現有絲分裂跡象,證明其保留增殖能力(核心治療功能);
免疫保護驗證:與 2×105~5×105 個 /ml 的 U937 巨噬細胞共培養 48h,盡管巨噬細胞 7~8h 開始攻擊并形成包圍簇,但封裝 MSC 始終保持結構完整,證明其可抵御早期免疫反應。
問題 3:該微流體封裝系統在臨床轉化中,相比現有 MSC 治療方案(如直接注射、支架載體),具備哪些獨特的臨床優勢?
答案:具備三大臨床優勢,適配微創治療場景:
微創兼容性:微膠囊尺寸 28.2±3.7µm,可通過內窺鏡或局部注射給藥,規避傳統組織工程支架需外科植入的問題,適配骨關節炎(關節內注射)與心肌梗死(局部注射);
制造規范性:系統符合GMP 標準,組件可消毒且體積緊湊,可容納于潔凈室或手術室,解決現有方案制造流程不可控(如細胞劑量異質性)的問題;
材料安全性:采用 FDA 批準的藻酸鹽材料,無鈣交聯避免毒性,且微膠囊涂層厚度 18.9µm(1% 濃度僅 5µm),既保障免疫保護(48h 屏蔽巨噬細胞),又不影響細胞后續增殖與功能發揮(24h 破殼)。
關注我們了解更多內容
ELVEFLOW認證的中國授權經銷商:
上海跡亞國際商貿有限公司
Gaia China Co.,Ltd.
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






