Science新文分享:體內制備CART用于癌癥和自免免疫病的優勢
文章來源公眾號:Of Studies 作者:Of Studies
上個月底Science上線了一篇體內制備CAR-T的文章,第一單位就是6月底剛剛被艾伯維(AbbVie)以高達21億美元現金對價收購的Capstan Therapeutics,在前面分享過這個研究團隊在2022年發的一篇Science,CD5靶向的LNP體內生成CART細胞治療心肌纖維化,團隊里面有CAR-T大牛Carl H. June,2023年諾獎獲得者Drew Weissman等,把這篇新的文章再分享給大家:
技術關鍵點
- tLNP平臺設計
新型離子化脂質Lipid L829:顯著減少肝臟脫靶遞送,快速代謝,毒性更低。
CD8+ T細胞靶向:通過抗CD8抗體修飾LNP,精準遞送mRNA至CD8+細胞毒性T細胞(避免CD4+細胞引發細胞因子風暴)。
CD8+ T細胞靶向:通過抗CD8抗體修飾LNP,精準遞送mRNA至CD8+細胞毒性T細胞(避免CD4+細胞引發細胞因子風暴)。
-
mRNA優化
優化CAR(抗CD19)mRNA的UTR和密碼子,使表達效率提升10倍,功能更強(細胞毒性、增殖、細胞因子釋放)。
主要內容
1、可電離脂質L829(Ionizable lipid L829)可減少tLNP對肝臟的脫靶遞送
1、可電離脂質L829(Ionizable lipid L829)可減少tLNP對肝臟的脫靶遞送

A:tLNP由五類脂質構成,表面偶聯抗體(靶向配體),內包mRNA。
B:Benchmark LNP,強熒光信號在肝和脾,表明肝脫靶嚴重。L829-tLNP信號集中在脾臟,肝臟脫靶明顯降低。表明L829減少了肝非特異攝取,提高了靶向遞送效率。
C:L829在肝中清除更快,24小時基本排出;Benchmark脂質仍持續存在。表明L829具有更好的代謝與安全性特征。
D:L829組炎癥標志物水平明顯低于Benchmark組,說明L829誘導的全身炎癥反應更低,更安全。
E:L829組比Benchmark組表現出更低的肝酶升高,說明L829在非人靈長類(猴)中也表現出更好肝安全性。
F:比較CD5-LNP與 CD8-LNP,CD8-LNP高度集中在CD8+T細胞,幾乎無在其他細胞類型。CD5-LNP分布更廣,部分表達在CD4+T、B細胞、單核細胞中。說明CD8-LNP具有更強的靶向特異性。
CD5 抗體修飾的 tLNP 會有更大比例脫靶到非效應細胞,而 CD8能夠更精準地定位到 CD8⁺ T 細胞。
G:在人源化小鼠模型中,CD8-LNP成功將mRNA遞送至人源CD8⁺ T細胞,CD4表達極低。
2、對anti-CD19的CAR mRNA的優化,提升了其在T細胞中的表達水平和功能活性。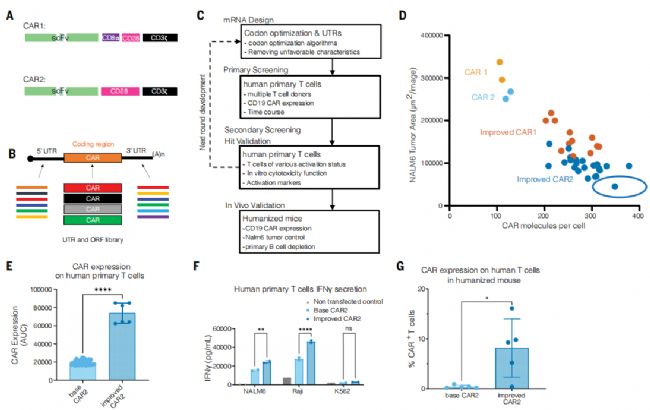

3、裝載B細胞靶向CAR的tLNP在自身免疫患者樣本和人源化小鼠中迅速誘導B細胞耗竭

4、使用裝載B細胞靶向CAR mRNA的tLNP治療,可在食蟹猴體內實現深度B細胞清除。
 3次給藥(0.5–2.0 mg/kg)可深度清除B細胞(外周血、脾臟、淋巴結),CAR+ CD8+ T細胞峰值達85%。
3次給藥(0.5–2.0 mg/kg)可深度清除B細胞(外周血、脾臟、淋巴結),CAR+ CD8+ T細胞峰值達85%。5、經tLNP治療實現全面B細胞清除后,B細胞譜系恢復過程中以初始B細胞為主。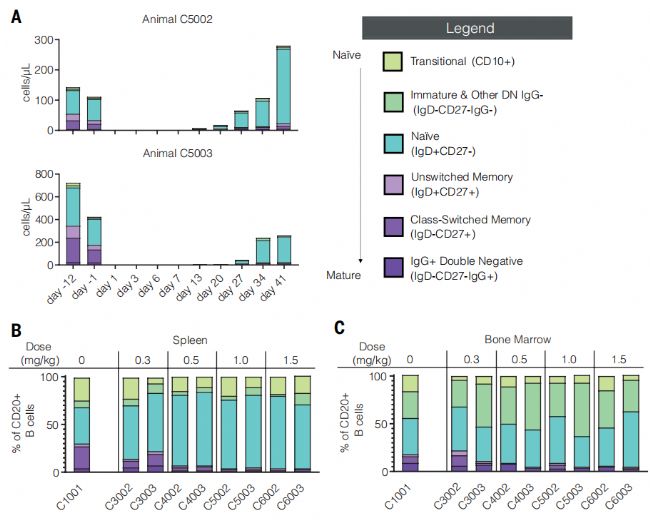

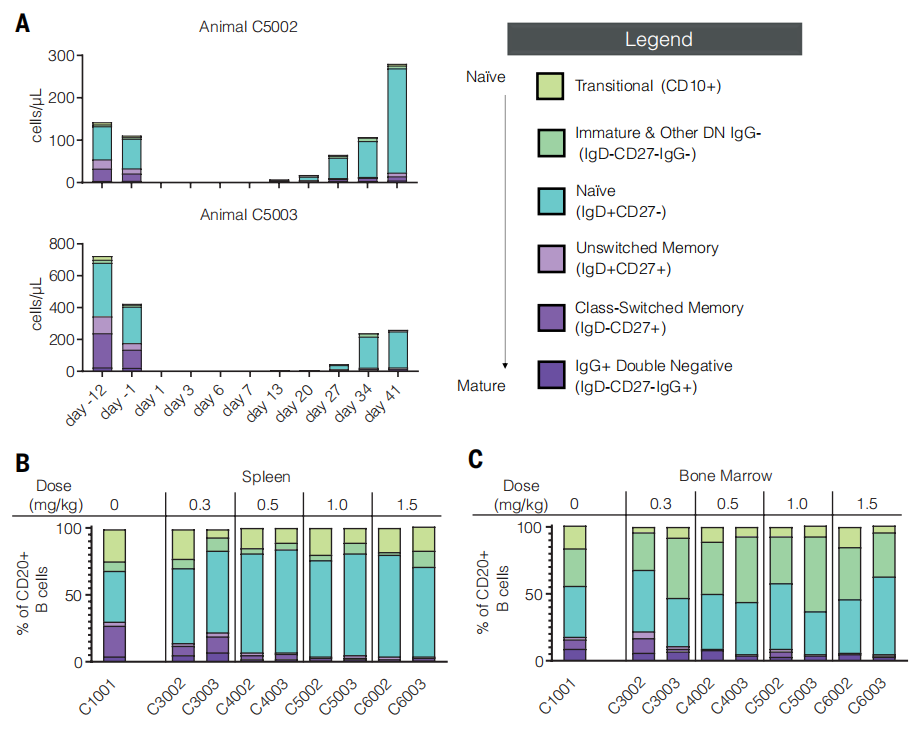
C1001、C3002、C4002 等是食蟹猴(cynomolgus monkey)實驗中的動物個體編號。
小結
tLNP能夠避免傳統CAR-T的淋巴清除毒性,擺脫專業化CAR-T中心限制,適用于大規模自身免疫病群體(全球約10%人口);mRNA瞬時表達,避免病毒載體導致的長期B細胞缺失或繼發惡性腫瘤;未來需探索長期重復給藥安全性、推進自身免疫病(如狼瘡)和B細胞惡性腫瘤的臨床試驗。
tLNP能夠避免傳統CAR-T的淋巴清除毒性,擺脫專業化CAR-T中心限制,適用于大規模自身免疫病群體(全球約10%人口);mRNA瞬時表達,避免病毒載體導致的長期B細胞缺失或繼發惡性腫瘤;未來需探索長期重復給藥安全性、推進自身免疫病(如狼瘡)和B細胞惡性腫瘤的臨床試驗。
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






