Luminex細(xì)胞因子檢測平臺助力肝移植缺血再灌注損傷機(jī)制研究
2025年1月,浙江大學(xué)醫(yī)學(xué)院附屬第二醫(yī)院研究團(tuán)隊(duì)在《Stem Cell Research & Therapy》(IF: 7.3)上發(fā)表題為《Mesenchymal stem cells-derived exosomes attenuate mouse non-heart-beating liver transplantation through Mir-17-5p-regulated Kupffer cell pyroptosis》的研究文章。該研究聚焦于心臟死亡供體(DCD)肝移植中缺血再灌注損傷(IRI)的關(guān)鍵機(jī)制,首次揭示間充質(zhì)干細(xì)胞外泌體(MSCs-Exo)通過miR-17-5p調(diào)控Kupffer細(xì)胞焦亡(pyroptosis),顯著改善移植肝存活率與功能,為緩解全球供肝短缺提供了新策略。

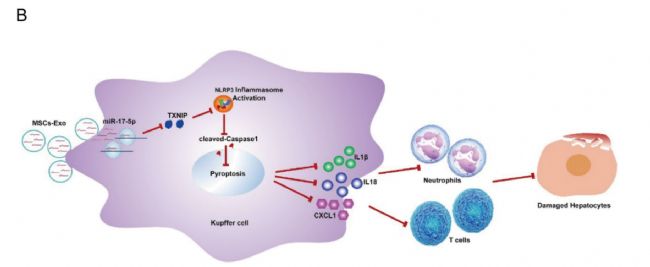
背景: 肝移植是終末期肝病最有效的治療方法。然而,供體肝臟的短缺已成為肝移植推進(jìn)的重大障礙。間充質(zhì)干細(xì)胞來源的外泌體 (MSCs-Exo) 已在肝病中得到廣泛研究。然而,它們?nèi)绾伪Wo(hù)心源性死亡 (DCD) 肝臟后器官捐獻(xiàn)的潛在機(jī)制仍不清楚。
方法: 該研究采用動脈化小鼠非心跳(NHB)肝移植模型研究MSCs-Exo對NHB肝移植的影響。研究其生存率、組織學(xué)、促炎細(xì)胞因子和趨化因子表達(dá)及其機(jī)制。
結(jié)果: 輸注MSCs-Exo減少了DCD肝移植物組織的損傷。體外和體內(nèi)實(shí)驗(yàn)表明,MSCs-Exo可以抑制過氧化氫誘導(dǎo)的庫普弗細(xì)胞焦亡。作者發(fā)現(xiàn)miR-17-5p在MSCs-Exo中顯著豐度,靶向和調(diào)控TXNIP表達(dá)。該作用通過經(jīng)典的Caspase1依賴性途徑抑制NLRP3介導(dǎo)的Kupffer細(xì)胞焦亡,減輕DCD肝移植物損傷。
結(jié)論: 該研究闡明了 MSCs-Exo 在 NHB 肝移植模型中的保護(hù)作用。該機(jī)制為MSCs-Exo在臨床應(yīng)用中改善肝移植質(zhì)量、緩解肝移植器官短缺問題提供了理論依據(jù)和新策略。
多因子檢測技術(shù)助力肝移植研究:
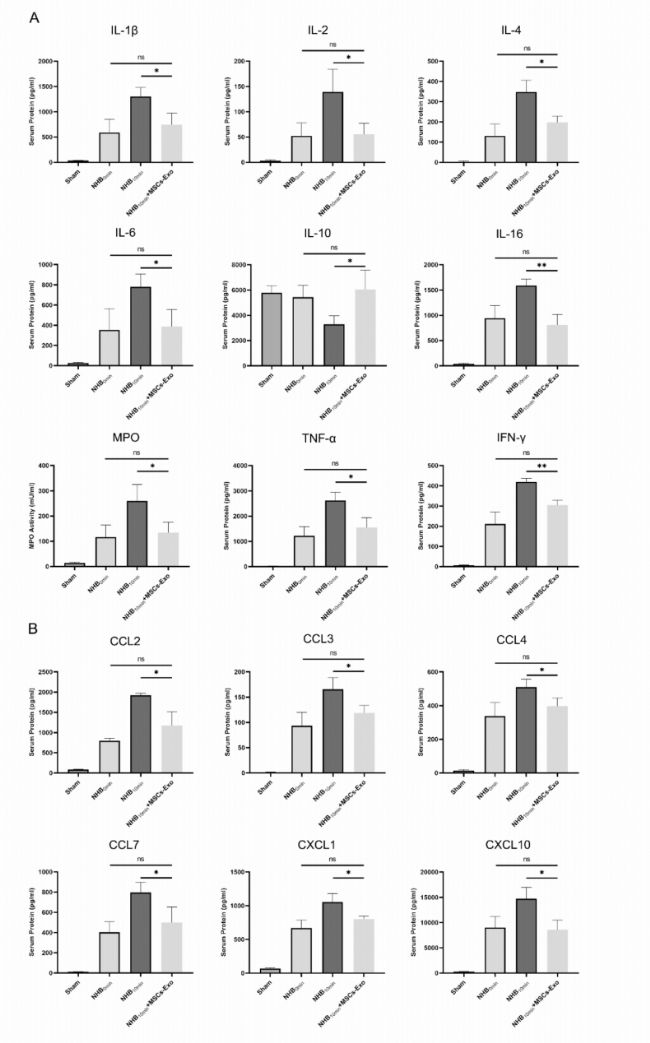
研究中,團(tuán)隊(duì)采用LabEx多因子液相芯片平臺(LX-MultiDTM-31),對移植后小鼠血清中31種炎癥因子與趨化因子進(jìn)行精準(zhǔn)定量。結(jié)果顯示,MSCs-Exo治療組顯著下調(diào)IL-1β、TNF-α、CXCL1等促炎因子,同時(shí)上調(diào)抗炎因子IL-10,證實(shí)其通過抑制Kupffer細(xì)胞焦亡-NLRP3炎癥小體通路阻斷級聯(lián)炎癥反應(yīng)。LabEx平臺的高靈敏度多靶點(diǎn)檢測能力,為闡明外泌體免疫調(diào)控機(jī)制提供了關(guān)鍵數(shù)據(jù)支持。
研究首次將MSCs-Exo的miRNA cargo與移植肝免疫微環(huán)境重塑關(guān)聯(lián),為DCD供肝質(zhì)量提升提供轉(zhuǎn)化醫(yī)學(xué)新思路。針對肝移植缺血再灌注損傷、慢性排斥反應(yīng)及器官功能修復(fù)等研究方向,樂備實(shí)(LabEx)提供多重細(xì)胞因子/趨化因子檢測全流程技術(shù)平臺,加速肝臟疾病機(jī)制研究與治療策略開發(fā)。“樂備實(shí)多重因子檢測平臺,正持續(xù)助力肝移植免疫調(diào)控與器官保護(hù)研究突破!”

- 微流控血腦屏障芯片的特征、設(shè)計(jì)方法及應(yīng)用領(lǐng)域
- Luminex細(xì)胞因子檢測平臺助力肝移植缺血再灌注損傷機(jī)制研究
- 類器官體積養(yǎng)不大的原因及解決方法
- 器官芯片技術(shù)在疾病治療新方式中的應(yīng)用及實(shí)驗(yàn)室使用基本要求
- 芯片上器官技術(shù)助力再現(xiàn)人體生理環(huán)境的方法
- 微流控芯片的材料、流體驅(qū)動方式及應(yīng)用
- 微流控技術(shù)的原理及液滴生成與操控方法
- 液相芯片助力巨噬細(xì)胞(TAMs)誘導(dǎo)胃癌發(fā)生淋巴結(jié)轉(zhuǎn)移的作用機(jī)制研究
- 點(diǎn)成直播:微流控技術(shù)驅(qū)動藥物發(fā)現(xiàn)與篩選的革新之路
- LabEx蛋白檢測拼板加速、抗體芯片"冰點(diǎn)"秒殺價(jià)促銷
- 因美納口碑芯片與設(shè)備服務(wù)攜多重禮遇限時(shí)開放
- 點(diǎn)成直播邀請:器官芯片如何賦能藥物研發(fā)與疾病研究
- 中美兩國制定最新法規(guī)推動“去動物化”實(shí)驗(yàn)落地
- Kirkstall QV類器官芯片落戶301解放軍總醫(yī)院
- M2生物芯片點(diǎn)樣儀聯(lián)動助力MADx過敏源檢測芯片生產(chǎn)
- 北京協(xié)和醫(yī)院邀請英國Kirkstall介紹器官芯片應(yīng)用






