scFv修飾的病毒樣顆粒遞送RNP實現(xiàn)體內(nèi)編輯T細胞
文章來源公眾號:Bloki 作者:Bloki

對LNP、病毒的靶向修飾是當下熱點,24年,諾獎得主Jennifer A. Doudna發(fā)過一篇Nature Biotechnology,用scFv修飾的病毒樣顆粒遞送RNP實現(xiàn)體內(nèi)基因編輯,具體內(nèi)容如下:
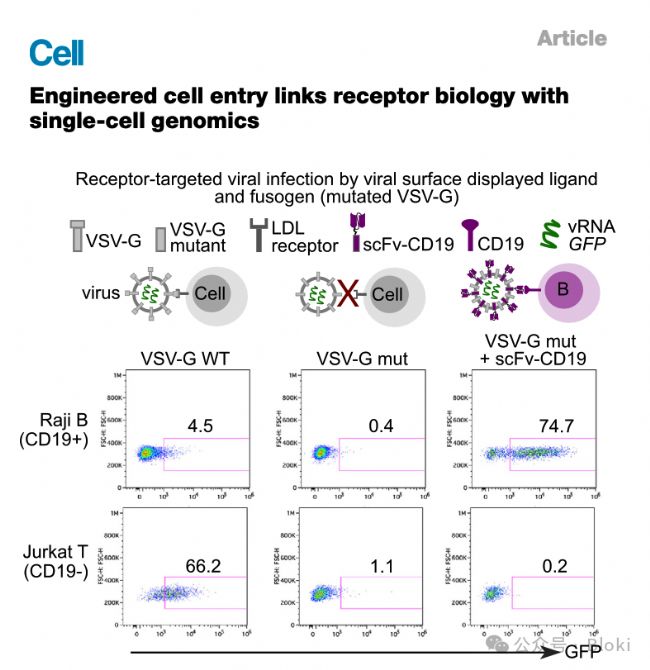
22年,一篇Cell用scFv+突變VSVG的病毒實現(xiàn)了細胞靶向遞送GFP
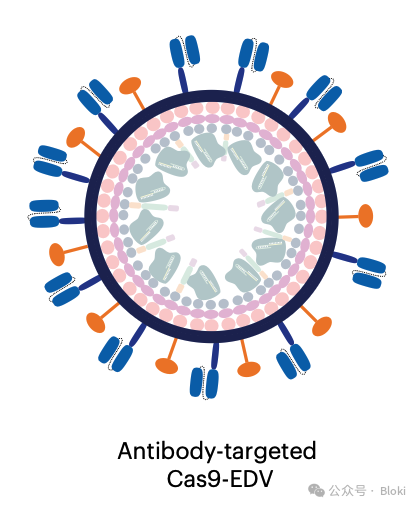
作者計劃用scFv(藍色)+突變VSVG(黃色)的病毒樣顆粒遞送RNP(Cas-gRNA復(fù)合物)
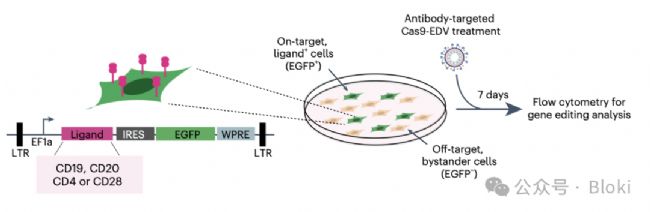
294T細胞同時表達EGFP和抗原,制備出工具靶細胞,和陰性細胞混合
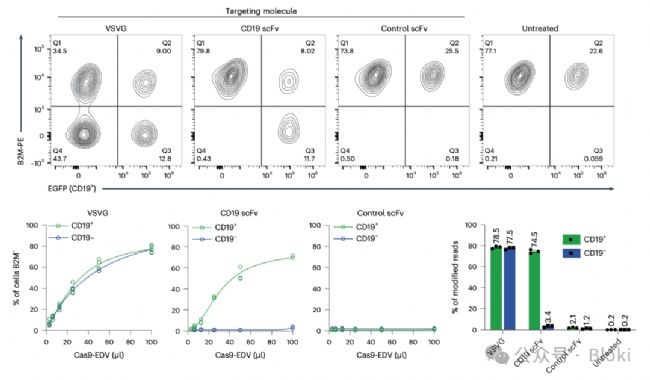
CD19 scFv修飾的病毒樣顆粒遞送敲B2M的RNP,特異性的敲CD19+細胞的B2M優(yōu)化,引入核轉(zhuǎn)運相關(guān)NES和NLS肽,提高編輯效率
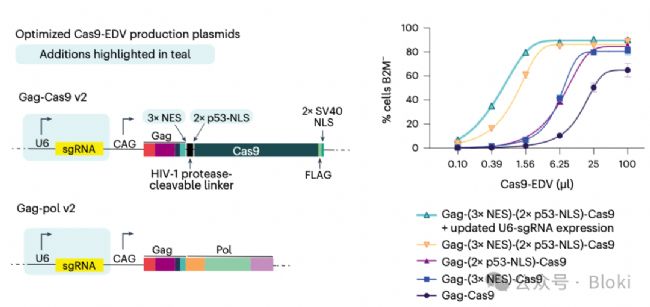
優(yōu)化后,不同細胞上均可高效實現(xiàn)基因編輯
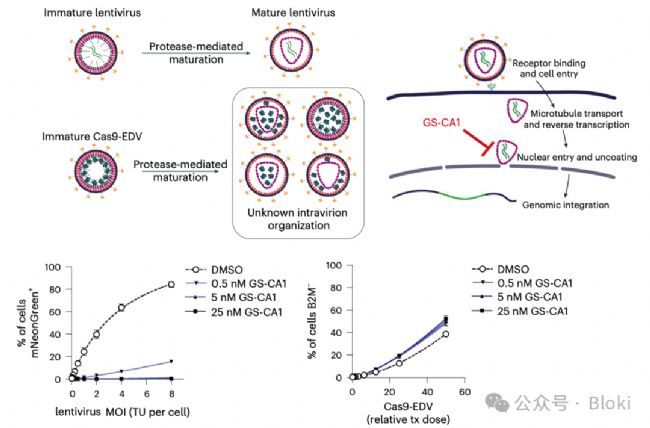
GS-CA1抑制病毒入核會影響慢病毒介導(dǎo)熒光蛋白表達,但不影響遞送RNP的病毒樣顆粒實現(xiàn)基因編輯(敲B2M)
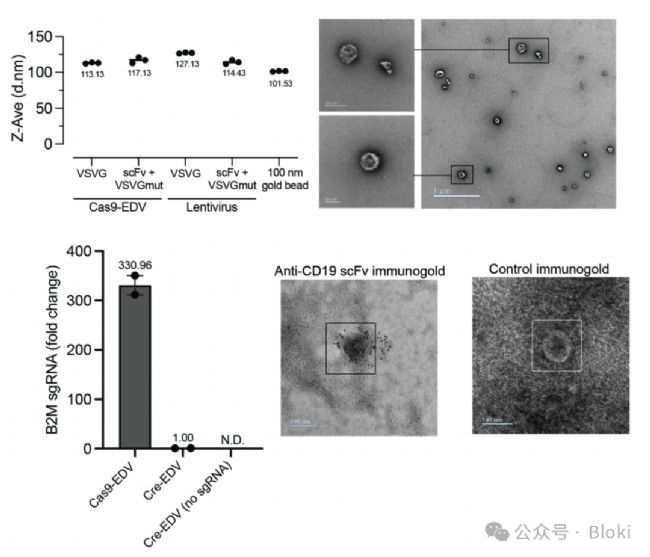
表征scFv修飾的病毒樣顆粒
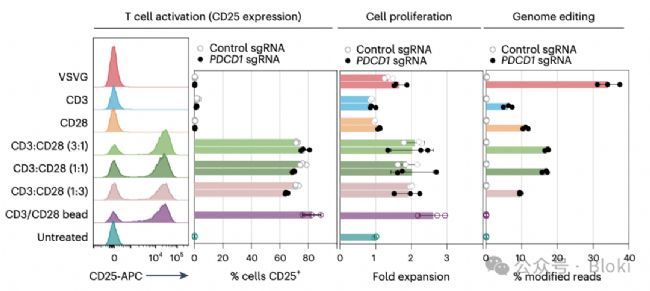
CD3、CD28 scFv修飾的病毒樣顆粒實現(xiàn)基因編輯的同時還可以促進T細胞激活、增殖
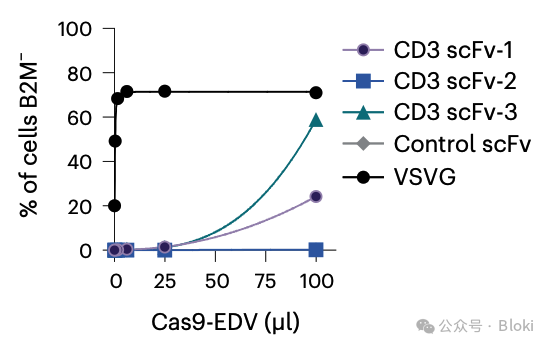
CD3 scFv修飾的病毒樣顆粒敲B2M
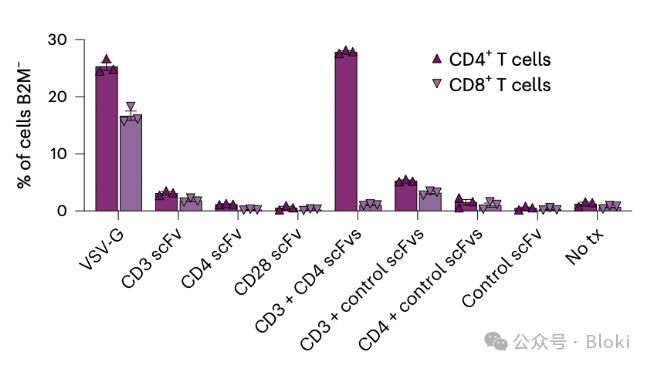
CD3、CD4雙scFv修飾的病毒樣顆粒高效、特異性敲CD4 T細胞的B2M – 雙靶向scFv修飾比較新穎,之前分享的一篇文章也用過類似策略可以體內(nèi)制備CAR-T的慢病毒
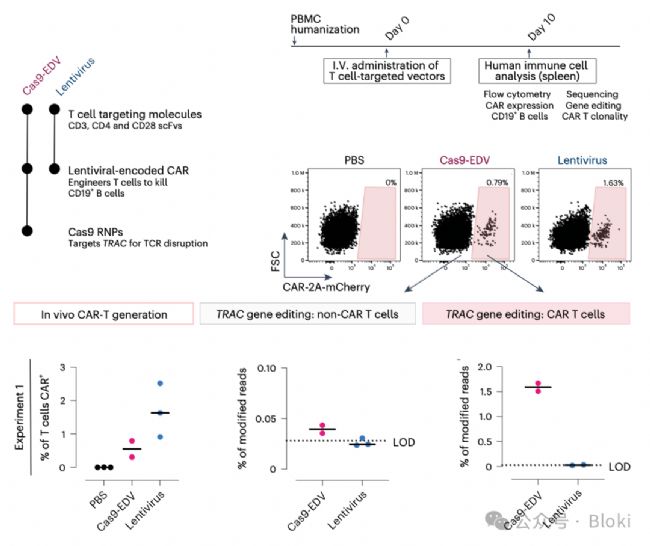
體內(nèi)介導(dǎo)CD19 CAR表達,實現(xiàn)基因編輯
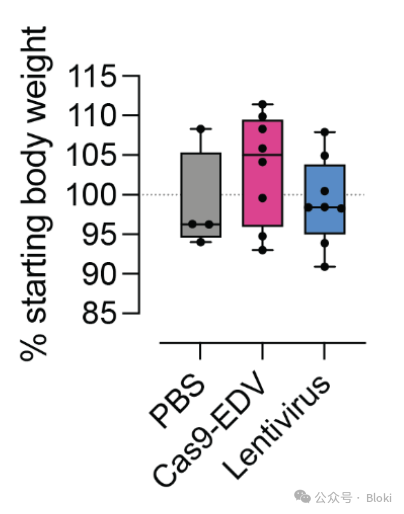
用小鼠體重初步說明安全性
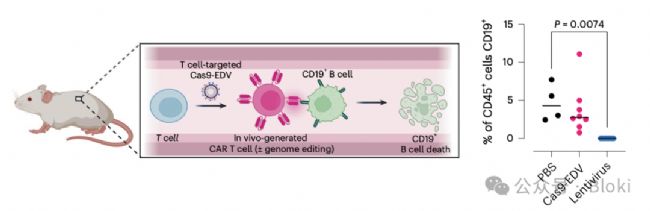
體內(nèi)搞掉部分B細胞
體內(nèi)制備CAR-T、體內(nèi)基因編輯都是熱點,雙scFv修飾的玩法值得關(guān)注,筆者還沒見到LNP上玩雙靶向。
- Hepcidin-25的作用機制及在炎癥、心血管與腫瘤等動物模型中的應(yīng)用
- Klotho蛋白的分子形式、功能及其在疾病與衰老進程中的核心作用
- 二甲雙胍(Metformin)在代謝、腫瘤、衰老與神經(jīng)疾病動物模型中的作用
- Romidepsin作為HDAC1/2抑制劑在細胞分化與損傷修復(fù)中的作用
- 白細胞介素-2(IL-2)的功能、信號調(diào)控機制及對免疫穩(wěn)態(tài)調(diào)控的雙面性
- 腫瘤/纖維化EMT研究中mIHC染色指標的組合及選擇方法
- Hepcidin-25(鐵調(diào)素)在鐵代謝與免疫反應(yīng)中的調(diào)節(jié)機制
- Vadimezan作為多功能STING激動劑與血管破壞劑的作用機制






