使用結晶紫生物膜定量檢測法測試新型噬菌體的抗菌特性
大腸桿菌是人類和動物腸道中常見的細菌,通常有助于維持健康的微生物群落。然而,一些大腸桿菌菌株具有致病性,可引發嚴重疾病,如泌尿道感染、腹瀉、腦膜炎和敗血癥。致病性大腸桿菌對現有常用抗生素的耐藥性日益增強。因此,迫切需要研發具有抗菌特性的全新藥物,或尋找替代方式來對抗這些感染。
噬菌體療法(phage therapy)是傳統抗生素的理想替代方案。噬菌體作為具有抗菌特性的病毒,能特異性感染細菌(導致細菌細胞溶解),且對人類或動物無任何不良影響。
在本研究中,研究人員從醫院廢水中分離并鑒定出一種新型噬菌體(APTC-EC-2A)。該噬菌體對多株抗生素耐藥的大腸桿菌表現出良好的抗菌活性。
然而,大腸桿菌(以及許多其他細菌)能夠形成生物膜,而生物膜通常比浮游細菌更具耐藥性。為評估APTC-EC-2A對細菌生物膜的抗菌特性,研究中采用了結晶紫生物膜質量定量法以及活/死菌活性檢測法。
1、結晶紫生物膜檢測法
結晶紫生物膜檢測法最早在30多年前發展應用起來,并在此后不斷經過改進。其核心步驟為:在96孔板底部培養細菌生物膜,并分別加入不同濃度的噬菌體(或其他抗菌劑)進行處理。隨后,殘留的黏附生物膜用結晶紫染色,未結合的染料洗去,再向孔內加入30%醋酸溶解結合的染料。通過測定上清液在595nm的吸光值,可以推算出生物膜的質量(圖 1)。
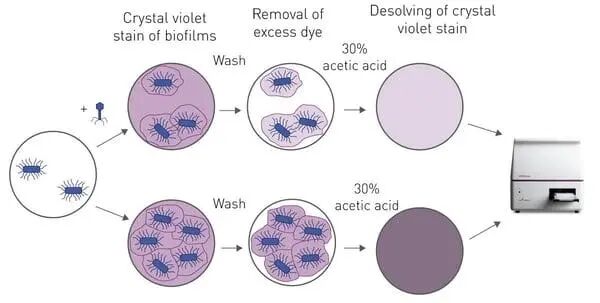 圖 1:抗菌特性檢測的原理示意圖。
圖 1:抗菌特性檢測的原理示意圖。
2、噬菌體效應測試
簡要流程如下:
將1McFarland單位的E. coli XL10生理鹽水懸液以1:15稀釋到LB培養基中。
在96孔板中,一列6個孔僅加入LB培養基作為陰性對照,其余孔加入150µL細菌懸液。
37°C培養48小時以促進生物膜形成,隨后用無菌1×PBS清洗兩次。
每孔加入200µL噬菌體溶液(濃度為5×10⁸pfu/mL或5×10⁹pfu/mL),LB培養基單獨作為陰性對照,LB+細菌懸液作為陽性對照。
37 °C再培養24小時。
噬菌體處理后,孔內用無菌PBS清洗,去除浮游菌。
每孔加入0.1%結晶紫200µL染色15分鐘,用蒸餾水沖洗并過夜風干。
每孔加入30%醋酸溶解染料,并測定595nm的吸光度。相對生物膜量通過與陽性對照吸光度比較獲得。
同樣的方法用于測試耐藥性的大腸桿菌菌株 ED、PC 和 378大腸桿菌菌株。
3、新型噬菌體降低生物膜生物量
結果顯示,所測試的噬菌體具有顯著的抗生物膜特性,且隨劑量增加,生物膜生物量呈劑量依賴性下降。
當 APTC-EC-2A 終濃度為1×10⁹ pfu時,明顯降低了XL10 Gold、ED、PC和378菌株的生物膜質量,相比未處理對照具有統計學顯著差異(圖 2)。
-
當終濃度為1×10⁸pfu時,生物膜質量最高下降53%(范圍 16–54%)。
-
當終濃度為1×10⁹pfu時,生物膜質量最高下降70%(范圍 27–70%)。
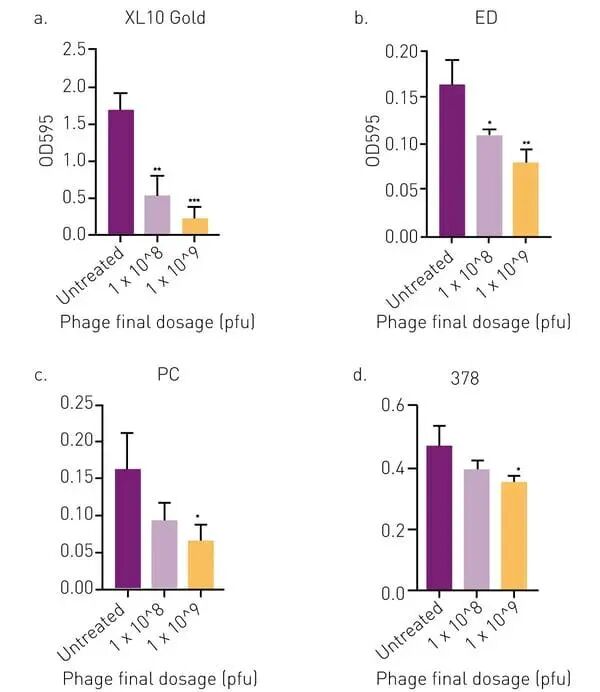 圖 2:結晶紫生物膜檢測結果。測定 E. coli 不同菌株的生物膜質量(OD 595),與未處理對照比較,驗證噬菌體的抗菌特性。
圖 2:結晶紫生物膜檢測結果。測定 E. coli 不同菌株的生物膜質量(OD 595),與未處理對照比較,驗證噬菌體的抗菌特性。
采用LIVE/DEAD BacLight細菌存活性試劑盒來確定APTC-EC-2A噬菌體處理后E. coli細胞中存活(SYTO9,綠色)與死亡(PI,紅色)細胞的百分比。在APTC-EC-2A處理的生物膜中,E. coli XL10、ED和PC的死亡細胞百分比在兩種噬菌體濃度下均較未處理對照有統計學顯著增加。然而,對于E. coli 378,僅在最高濃度的APTC-EC-2A處理下才觀察到與對照相比顯著增加的細胞死亡率和抗菌特性(圖 3)。
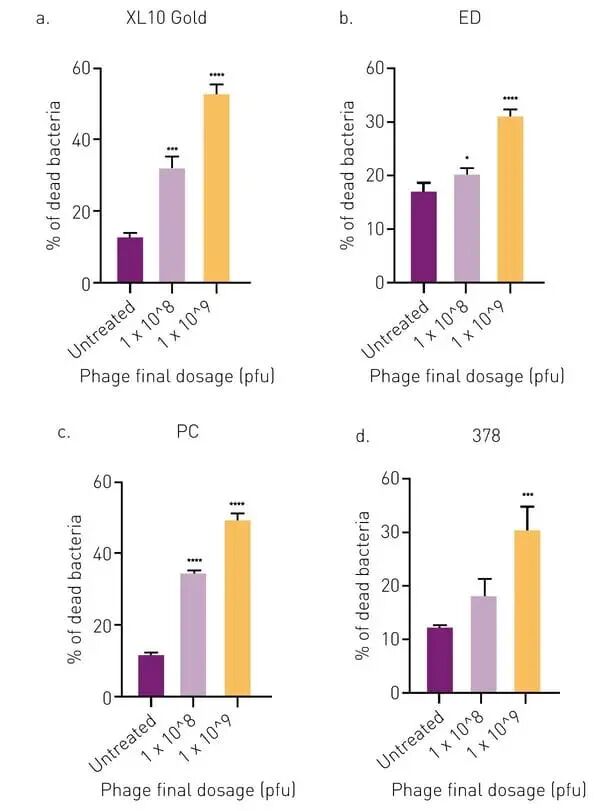 圖 3:活/死菌檢測結果。通過共聚焦激光顯微鏡計數XL10 Gold(A)、ED(B)、PC(C)及378(D)菌株培養物中的死亡細胞百分比,評估抗菌特性。
圖 3:活/死菌檢測結果。通過共聚焦激光顯微鏡計數XL10 Gold(A)、ED(B)、PC(C)及378(D)菌株培養物中的死亡細胞百分比,評估抗菌特性。
結論
本研究發現了一種對耐藥性大腸桿菌具有抗菌活性的新型噬菌體。其廣譜溶解活性及在寬pH值和溫度范圍內的穩定性,使其成為推進臨床前及臨床開發的有前景候選物。
BMG LABTECH系列酶標儀多年來廣泛應用于細菌生長檢測。該設備可實現生長動力學曲線測定,并能根據需求提供培養功能及長期高強度振蕩。所有儀器均配備固態CCD分光計,可進行220-1000nm波段的吸光度測量,使其成為測定抗菌藥物及其他藥物的理想平臺。
References
-
Hon,K., et al. APTC-EC-2A: A Lytic Phage Targeting Multidrug Resistant E. coli- Planktonic Cells and Biofilms. Microorganisms, 2022, 10, 102.
-
Staneva, A.D., et al. Antibiofouling Activity of Graphene Materials and Graphene-Based Antimicrobial Coatings. Microorganisms 2021, 9, 1839.
-
Stepanovic, S., et al. A modified microtiter-13 plate test for quantification of staphylococcal biofilm formation. J Microbiol Methods, 40 14 (2000) 175.
轉載自:BMG LABTECH
回復:BMG,查看更多相關視頻
長按/掃描以下二維碼可識別關注公眾號

廣州進科馳安科技有限公司
Bio-Gene Technology Limited
熱線:176 2009 3784
www.bio-gene.com.cn
marketing@bio-gene.com.cn
香港 北京 上海 廣州






