通過PK和PD實驗研究不同Fc功能突變體對于ADC藥效活性的影響
文章來源公眾號:ATCG 作者:ATCG
眾所周知,大部分ADC的MoA是靶向腫瘤細胞,然后實現payload的殺傷功能。然而,有些ADC的分子設計會保留其裸抗部分的Fc功能活性,有些會將其突變失效。那么,具有Fc功能活性的ADC的藥效,究竟是源于payload,還是源于裸抗的Fc效應呢?一起來看看吧!
DOI鏈接:https://doi.org/10.1208/s12248-024-00998-4

圖1 思維導圖

ADC對Fc端的設計
ADC藥物的治療窗口很狹窄(在保證安全性的劑量范圍內起作用),因此人們將目光對準了裸抗部分——裸抗具有的Fc功能帶來的免疫效應和ADC的相互作用可能會提高ADC藥物的治療窗口。以下是一些已上市的ADC藥物對EF(Effector function)的改造策略以及帶來的藥效或副作用結果:
那Fc功能如何影響PK/PD呢?以下是一些實驗設計和數據。
體外和體內藥效數據
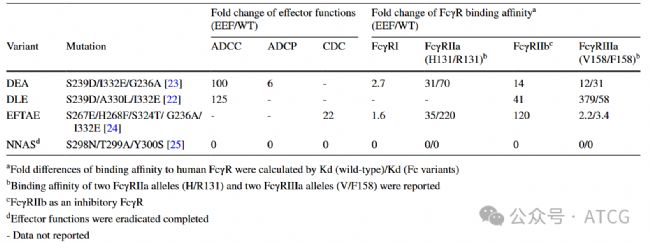
基于以往研究數據,研究團隊針對于曲妥珠單抗-vc-MMAE設計了一系列Fc端序列突變以增強/減弱Fc功能。如下表所示:
表2 不同位點的Fc序列突變
然后,如圖2所示,進行了一系列的體外實驗、體內的PK和PD實驗,以及進行了PK/PD的建模,得出了不同Fc功能突變體對于ADC活性的協同參數φ。
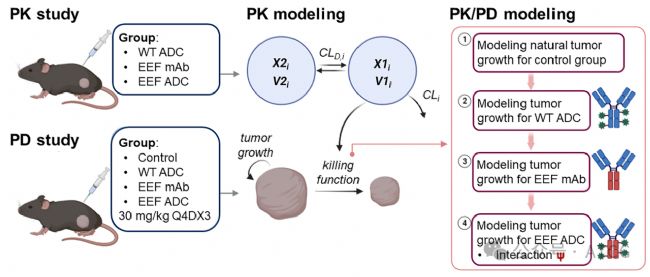
圖2 Fc功能研究示意圖和PK/PD建模方法
體外實驗結果:從體外細胞活性實驗(ADCC為例)可看出,Fc增強突變體-DEA和DLE有效增強了ADCC效應,并且對ADC的細胞毒性沒有影響。并且通過IC50可以看出,人源靶細胞比鼠源靶細胞對于ADC更為敏感,此處涉及到給藥劑量計算。
(其實在此有個疑問,即Trastuzumab 應該具有高的ADCC活性,但是在此實驗中,ADCC殺傷率僅為20%左右,有可能由于實驗參數以及使用PBMC的緣故?)

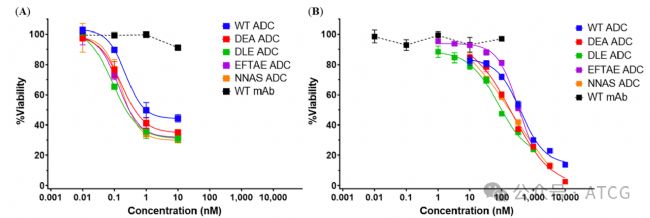
圖4 Fc突變體的細胞毒性實驗
PK實驗結果:
PK實驗使用了攜帶D5-HER2腫瘤的C57BL / 6小鼠,給藥(wtADC,wt裸抗,突變體裸抗,突變體ADC)后,使用ELISA測定不同時間點血漿中藥物濃度。圖5結果顯示,同一突變體的ADC和裸抗的PK相似。Fc減弱突變體ADC與wtADC的結果相當,但Fc增強突變體DEA和DLE 的AUC減少65%,清除率增加3倍,Vss(穩態分布容積)增加兩倍。說明Fc增強突變體增加了ADC的系統暴露量和藥物處置(disposition)。
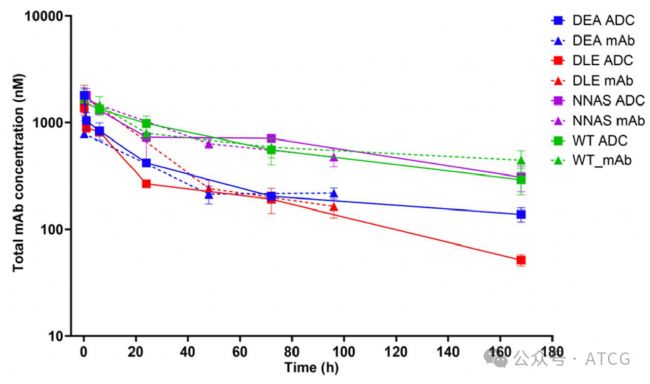
圖5 Fc突變體的PK實驗
后續證實,Fc增強突變體ADC并沒有改變與FcRn的結合,而可能通過FcγR相互作用,導致在富含FcγR的組織(例如肝臟和脾臟)中快速分布和顯著積累。Vss增加反應了腫瘤微環境中Fc增強突變體的清除率更高或產生更高的內化。Fc增強的ADC更容易收到Fc介導的免疫細胞全身和局部的攝取和降解,從而導致清除率更高。PD實驗結果:
PD實驗通過荷瘤實驗,當腫瘤體積增長到150mm3時,每四天靜脈注射大于30mg/kg藥物,共給三次,隔天測定腫瘤體積,并稱體重排除顯著毒性。可以看出,Fc增強突變顯示出比Fc減弱突變與wt更強的抑瘤效應。
可通過以下縝密的推論得出給藥劑量和頻率:1️⃣ 根據ADC體外細胞毒性活性數據,主要是小鼠靶細胞(對ADC更不敏感)的IC50確定給藥劑量 2️⃣ 除payload活性外,還需考慮Fc端活性 3️⃣ 此給藥方案在其他HER2高表達小鼠模型(N87)中有成功案例
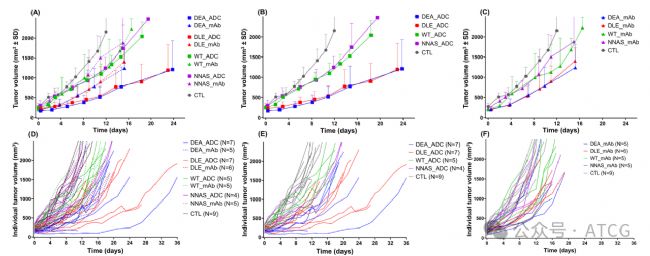
圖6 Fc突變體的PD實驗
從以上PK和PD的數據可以看出,雖然Fc增強突變體ADC導致AUC大幅降低,但增強了療效。這打破了“血藥濃度越高,療效越好”的簡單線性思維。
接下來到這篇文章的創新部分——開發并應用了一套定量的PK/PD建模框架,首次將Fc功能的“協同貢獻”與Payload的殺傷效應分離開來,并賦予了一個可計算的數值(ψ)。這個初始概念來源于評估聯合給藥的協同/疊加/拮抗的PK/PD建模。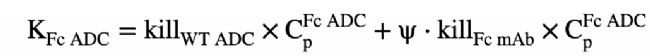
公式的前半部分代表payload產生的細胞毒性作用,與血漿濃度(Cp)相關(此處假設payload與WT ADC的細胞毒性相同,因此引用的是Kill WT ADC),后半部分引入ψ,描述Fc工程化改造的ADC的效力。其中Kill WT ADC和Kill Fc mab均為常數,分別通過擬合WT ADC組和裸抗組的藥效數據得出。
簡單來講:
- 若ψ=1 表示 Fc殺傷與ADC毒性相互獨立(即藥效簡單相加模型)
- 若ψ>1 揭示Fc功能與ADC毒性存在協同機制(即藥效1+1>2模型)
- 若ψ<1 揭示Fc功能與ADC毒性存在某種干擾
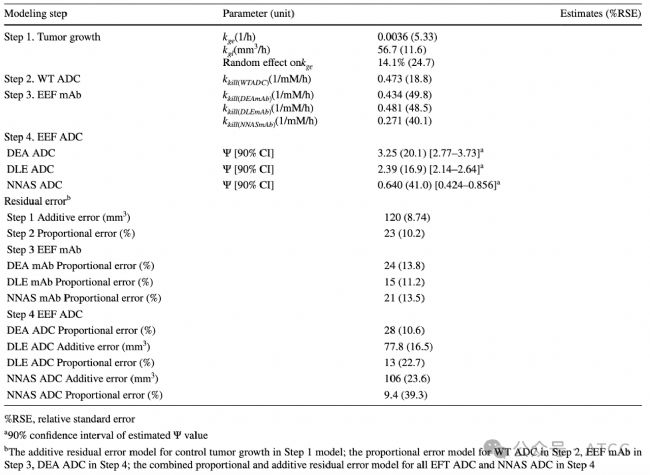
結果如下表所示,Fc增強突變DEA-ADC(ψ=3.25),DLE-ADC(ψ=2.39),Fc減弱突變NNAS-ADC(ψ=0.64)。解釋一下就是:對于DEA和DLE ADC,Fc效應功能在ADC上的效果是它們作為獨立裸抗時的3.25倍和2.39倍,說明具有協同作用;對于NNAS ADC,消除Fc功能后,其療效比單純的Payload殺傷+無Fc功能還要差(ψ < 1)。
Fc增強功能:安全性和療效的平衡
以上Fc增強體ADC的療效自不用多說,但同時也是在刀尖上跳舞,可能會帶來以下安全性風險:
-
“脫靶毒性”風險增加:Vss的增大提示ADC可能更多分布于肝、脾等FcγR富集的正常組織,可能導致這些組織的損傷。
-
免疫相關毒性風險:強烈激活免疫系統可能引發細胞因子釋放綜合征或類似免疫檢查點抑制劑的免疫相關不良事件。
-
“on-target, off-tumor”毒性加劇:如果靶點在正常組織有低水平表達,增強的Fc功能可能會引導免疫細胞對這些正常組織進行攻擊,放大靶向毒性。






