超分辨率顯微鏡技術解析:以更多細節研究亞細胞結構與動態
以空前的細節探索生命的真實本質
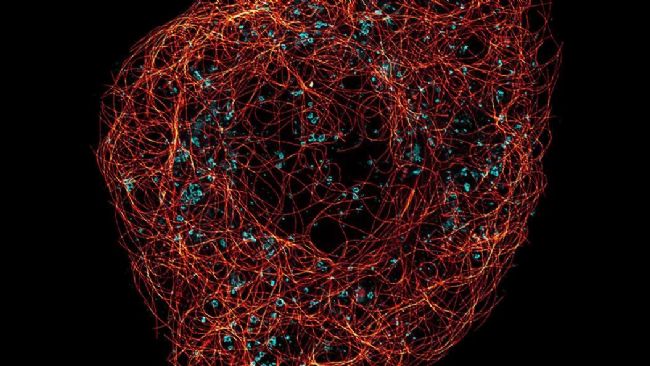
超分辨率光學顯微鏡使您能夠以更多的細節研究亞細胞結構和動態。使用 LIGHTNING 技術時,共聚焦圖像采集的空間分辨率提高了一倍,而使用 STED 時可以在納米尺度上提供洞察。了解更多關于徠卡顯微系統超分辨率方法的信息,以及它們如何在病毒學、免疫學、神經科學和癌癥研究領域推動新發現。
關于超分辨率
超分辨率顯微鏡與電子顯微鏡有什么區別?
超分辨率顯微鏡利用可見光光學來可視化樣本,而電子顯微鏡則利用電子束對樣本進行成像。這兩種技術各有優缺點,但只有超分辨率顯微鏡提供了對活體標本進行實驗、標記多個分子靶標以賦予其特定對比度以及方便樣本準備的優勢。
相關產品

超分辨率光學顯微鏡使您能夠以更多的細節研究亞細胞結構和動態。使用 LIGHTNING 技術時,共聚焦圖像采集的空間分辨率提高了一倍,而使用 STED 時可以在納米尺度上提供洞察。了解更多關于徠卡顯微系統超分辨率方法的信息,以及它們如何在病毒學、免疫學、神經科學和癌癥研究領域推動新發現。
什么是超分辨率顯微鏡?
超分辨率顯微鏡是一種光學成像技術,克服了光的衍射極限,允許以比傳統光學顯微鏡更多的細節可視化亞細胞結構和動態。使用 STED(受激發射損耗)和納米成像可以實現 30 納米的分辨率。納米級分辨率揭示了關于亞細胞結構和相互作用的更多細節信息。
超分辨率顯微鏡在病毒學、免疫學、神經科學和癌癥研究領域推動了突破性的發現。
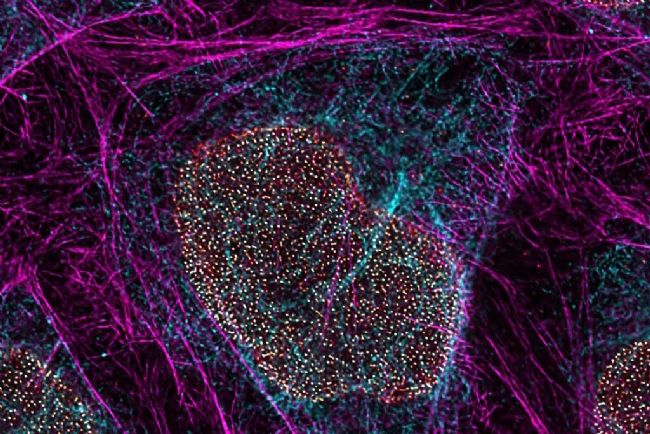 用于細胞生物學應用的多彩 TauSTED Xtend 775,要求對多個細胞組分進行納米級分辨率成像。細胞顯示出波形蛋白纖維(AF 594)、肌動蛋白網絡(ATTO 647N)和核孔籃(CF 680R)。樣本由布里吉特·貝爾格納、馬里亞諾·岡薩雷斯·皮斯菲爾、斯特芬·迪特策爾提供,生物醫學中心生物成像核心設施,路德維希-馬克西米利安大學,德國慕尼黑。
用于細胞生物學應用的多彩 TauSTED Xtend 775,要求對多個細胞組分進行納米級分辨率成像。細胞顯示出波形蛋白纖維(AF 594)、肌動蛋白網絡(ATTO 647N)和核孔籃(CF 680R)。樣本由布里吉特·貝爾格納、馬里亞諾·岡薩雷斯·皮斯菲爾、斯特芬·迪特策爾提供,生物醫學中心生物成像核心設施,路德維希-馬克西米利安大學,德國慕尼黑。
超分辨率顯微鏡在病毒學、免疫學、神經科學和癌癥研究領域推動了突破性的發現。
 用于細胞生物學應用的多彩 TauSTED Xtend 775,要求對多個細胞組分進行納米級分辨率成像。細胞顯示出波形蛋白纖維(AF 594)、肌動蛋白網絡(ATTO 647N)和核孔籃(CF 680R)。樣本由布里吉特·貝爾格納、馬里亞諾·岡薩雷斯·皮斯菲爾、斯特芬·迪特策爾提供,生物醫學中心生物成像核心設施,路德維希-馬克西米利安大學,德國慕尼黑。
用于細胞生物學應用的多彩 TauSTED Xtend 775,要求對多個細胞組分進行納米級分辨率成像。細胞顯示出波形蛋白纖維(AF 594)、肌動蛋白網絡(ATTO 647N)和核孔籃(CF 680R)。樣本由布里吉特·貝爾格納、馬里亞諾·岡薩雷斯·皮斯菲爾、斯特芬·迪特策爾提供,生物醫學中心生物成像核心設施,路德維希-馬克西米利安大學,德國慕尼黑。關于超分辨率
由于光的衍射極限,“傳統”的熒光顯微鏡技術無法分辨低于 240 納米的結構。因為生物學并不止步于這個尺度,因此所謂的超分辨率顯微鏡技術是不可或缺的。LIGHTNING 和 STED 是兩種引人注目的徠卡顯微系統超分辨率共聚焦方法,用于以更高的精度展示結構,并揭示無法看到的細節。
LIGHTNING 檢測概念基于自適應去卷積,有效地將橫向分辨率提高到 120 納米。使用 LIGHTNING,您可以探測從微管動態到亞細胞區室結構的樣本。
STED 納米顯微鏡將超分辨率提升到一個新的水平,使您能夠常規地實現低于 30 納米的橫向分辨率。通過 STED,您可以在體內剖析細胞結構和功能,例如染色質和核孔的重組、神經元結構的微小變化、線粒體和突觸囊泡的細胞內運輸、病毒顆粒的進入、蛋白質復合物的共定位等。
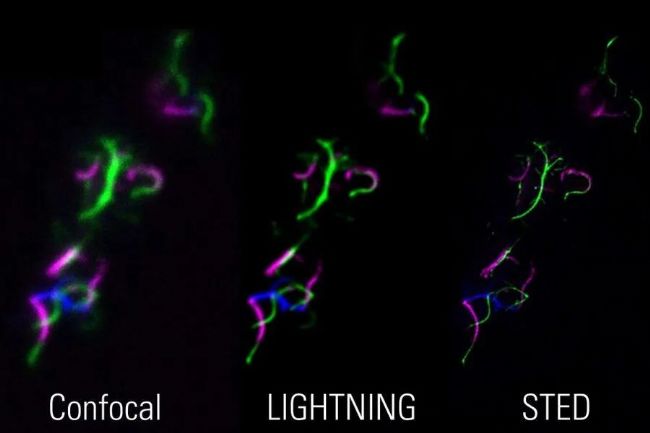 細菌鞭毛的圖像:相關的三色共聚焦-LIGHTNING-STED 成像允許同時使用互補的方法來研究和驗證樣本。樣本由德國柏林洪堡大學的 Marc Erhardt 提供。
細菌鞭毛的圖像:相關的三色共聚焦-LIGHTNING-STED 成像允許同時使用互補的方法來研究和驗證樣本。樣本由德國柏林洪堡大學的 Marc Erhardt 提供。
LIGHTNING 檢測概念基于自適應去卷積,有效地將橫向分辨率提高到 120 納米。使用 LIGHTNING,您可以探測從微管動態到亞細胞區室結構的樣本。
STED 納米顯微鏡將超分辨率提升到一個新的水平,使您能夠常規地實現低于 30 納米的橫向分辨率。通過 STED,您可以在體內剖析細胞結構和功能,例如染色質和核孔的重組、神經元結構的微小變化、線粒體和突觸囊泡的細胞內運輸、病毒顆粒的進入、蛋白質復合物的共定位等。
 細菌鞭毛的圖像:相關的三色共聚焦-LIGHTNING-STED 成像允許同時使用互補的方法來研究和驗證樣本。樣本由德國柏林洪堡大學的 Marc Erhardt 提供。
細菌鞭毛的圖像:相關的三色共聚焦-LIGHTNING-STED 成像允許同時使用互補的方法來研究和驗證樣本。樣本由德國柏林洪堡大學的 Marc Erhardt 提供。超分辨率顯微鏡是如何工作的?
超分辨率顯微鏡可以通過多種方式進行。
● LIGHTNING 檢測概念使超分辨率共聚焦顯微鏡成為可能。與傳統的去卷積技術使用全圖像的全局參數集不同,它基于一種自適應去卷積過程,該過程使用體素特定的決策掩模來尋找合適的去卷積參數。得益于強大的 GPU 計算,LIGHTNING 能夠在近實時的情況下同時處理多種顏色。結合共振掃描儀,它還提供了大視場和高幀率。
● LIGHTNING 檢測概念使超分辨率共聚焦顯微鏡成為可能。與傳統的去卷積技術使用全圖像的全局參數集不同,它基于一種自適應去卷積過程,該過程使用體素特定的決策掩模來尋找合適的去卷積參數。得益于強大的 GPU 計算,LIGHTNING 能夠在近實時的情況下同時處理多種顏色。結合共振掃描儀,它還提供了大視場和高幀率。
● 受激發射損耗(STED)方法與共聚焦技術結合,可實現超分辨率熒光顯微術。STED支持多通道成像,并在三維空間內實現各向同性的超分辨率成像。其原理基于:使用激發熒光團的波長照射衍射極限光斑,同時以引發退激發或受激發射的波長照射環形區域。此設計使僅有亞衍射區域處于激發態,從而實現比傳統衍射極限光學顯微術更高的分辨率。徠卡顯微系統的獨特TauSTED功能可在提升STED分辨率的同時,消除不必要的背景噪聲。
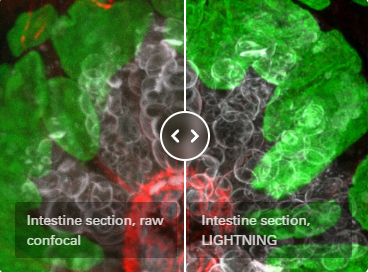
FluoCells 小鼠腸道切片。杯狀細胞的粘液,灰色,Alexa Fluor 350 WGA。細胞核,綠色,SYTOX Green。絲狀肌動蛋白,紅色,Alexa Fluor 568 phalloidin。

FluoCells 小鼠腸道切片。杯狀細胞的粘液,灰色,Alexa Fluor 350 WGA。細胞核,綠色,SYTOX Green。絲狀肌動蛋白,紅色,Alexa Fluor 568 phalloidin。
超分辨率顯微鏡與電子顯微鏡有什么區別?
超分辨率顯微鏡利用可見光光學來可視化樣本,而電子顯微鏡則利用電子束對樣本進行成像。這兩種技術各有優缺點,但只有超分辨率顯微鏡提供了對活體標本進行實驗、標記多個分子靶標以賦予其特定對比度以及方便樣本準備的優勢。
相關產品
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com







