實驗性自身免疫性腦脊髓炎(EAE)模型的建立與評估
一、實驗性自身免疫性腦脊髓炎(EAE)概述
二、動物選擇
三、建模方法
(一)主動誘導法
(二)被動轉移實驗
四、模型判定標準
(一)神經功能評分
五、以小鼠為例的MOG誘導EAE模型建立
前期準備
1、完全弗氏佐劑(CFA)的配制:將結核分枝桿菌加入弗氏不完全佐劑(IFA)中,充分混勻后置于4℃冰箱備用。
2、百日咳毒素儲存液(PTX)的配制:將百日咳毒素溶解于PBS中,儲存于4℃冰箱。
3、抗原佐劑乳化物的制備:將MOG 35-55多肽與CFA混合乳化,形成油包水混合物。
模型制備
1、動物選擇:選擇6-8周齡、18-25克的雌性C57BL/6小鼠,確保品系純正和SPF級飼養環境。
2、注射與處理:
六、結語
實驗性自身免疫性腦脊髓炎(EAE)是一種以特異性致敏的CD4+T細胞介導為主的自身免疫性疾病,其病理變化與多發性硬化(MS)類似。EAE模型是研究MS病理過程和發病機制的重要工具,在臨床神經免疫學研究中具有重要意義。

二、動物選擇
多種動物可用于EAE模型的建立,包括雞、小鼠、大鼠、豚鼠、家兔、羊、犬和猴等。不同種屬或品系的動物對EAE的敏感性存在顯著差異。常用的敏感動物包括Lewis和DA大鼠、PL/J和SJL/J小鼠以及Hartley和Strain13豚鼠等。小鼠和大鼠的EAE模型在臨床表現、病理和免疫等方面與人類脫髓鞘疾病較為相似,因此應用最為廣泛。
三、建模方法
(一)主動誘導法
主動誘導法是通過將抗原與佐劑混合后注射到動物體內,經過一定時間的潛伏期誘導EAE的產生。常用的致敏抗原有髓鞘堿性蛋白(MBP)、蛋白脂(PLP)、髓寡樹突細胞糖蛋白(MOG)等。
1、抗原與佐劑的混合:抗原需與佐劑(如完全弗氏佐劑,CFA)混合制成乳劑。CFA能提高抗原的免疫反應強度并延長免疫時間,而百日咳毒素(PTX)可增加血管通透性,促進T細胞通過血腦屏障。
2、注射途徑:常用的注射途徑包括皮下、腹腔和尾靜脈等,其中皮下多點注射和腳墊注射的發病率較高。
1、抗原與佐劑的混合:抗原需與佐劑(如完全弗氏佐劑,CFA)混合制成乳劑。CFA能提高抗原的免疫反應強度并延長免疫時間,而百日咳毒素(PTX)可增加血管通透性,促進T細胞通過血腦屏障。
2、注射途徑:常用的注射途徑包括皮下、腹腔和尾靜脈等,其中皮下多點注射和腳墊注射的發病率較高。
(二)被動轉移實驗
被動轉移實驗通過將EAE抗原特異反應性T細胞轉輸給同一品系的健康動物,使其發病。這是研究EAE發病機制的直接證據,也是研究治療和預防措施的良好模型。

四、模型判定標準
(一)神經功能評分
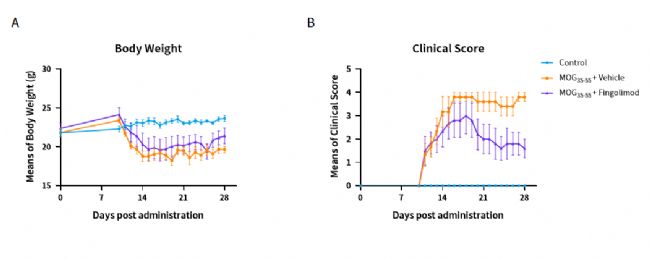
根據Kono等提出的標準,神經功能評分分為5級:1級為尾部無力,2級為尾部無力加肢體無力,3級為肢體輕度麻痹,4級為肢體嚴重麻痹,5級為瀕死狀態。
(二)病理檢測結果
通過HE染色等方法檢查中樞神經系統的炎癥和脫髓鞘情況。EAE模型組小鼠脊髓中可見大量炎性細胞聚集,髓鞘結構松散、崩解,密度降低。
(三)免疫熒光雙染結果
EAE模型組小鼠脊髓中活化的小膠質細胞數量增多,而活化星形膠質細胞數量減少。
(四)細胞流式分析
EAE模型小鼠中致炎細胞Th17數量顯著增加,抑炎細胞Treg和Breg數量顯著降低。
五、以小鼠為例的MOG誘導EAE模型建立
前期準備
1、完全弗氏佐劑(CFA)的配制:將結核分枝桿菌加入弗氏不完全佐劑(IFA)中,充分混勻后置于4℃冰箱備用。
2、百日咳毒素儲存液(PTX)的配制:將百日咳毒素溶解于PBS中,儲存于4℃冰箱。
3、抗原佐劑乳化物的制備:將MOG 35-55多肽與CFA混合乳化,形成油包水混合物。
模型制備
1、動物選擇:選擇6-8周齡、18-25克的雌性C57BL/6小鼠,確保品系純正和SPF級飼養環境。
2、注射與處理:
- 麻醉小鼠,對注射部位進行消毒。
- 每側皮下注射抗原佐劑乳化物100μl,隨后腹腔注射PTX。
- 48小時后再次腹腔注射PTX,第七天加強免疫。
六、結語
EAE模型是研究MS病理機制和治療方法的重要工具。通過優化建模方法和評估標準,EAE模型為揭示MS的發病機制和開發新的治療策略提供了有力支持。
杭州斯達特 (www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。
杭州斯達特 (www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






