深度解析2024年全球53款創(chuàng)新藥審批重塑難治性疾病治療格局
2024年全球新藥審批:53款創(chuàng)新藥如何重塑難治性疾病治療格局?
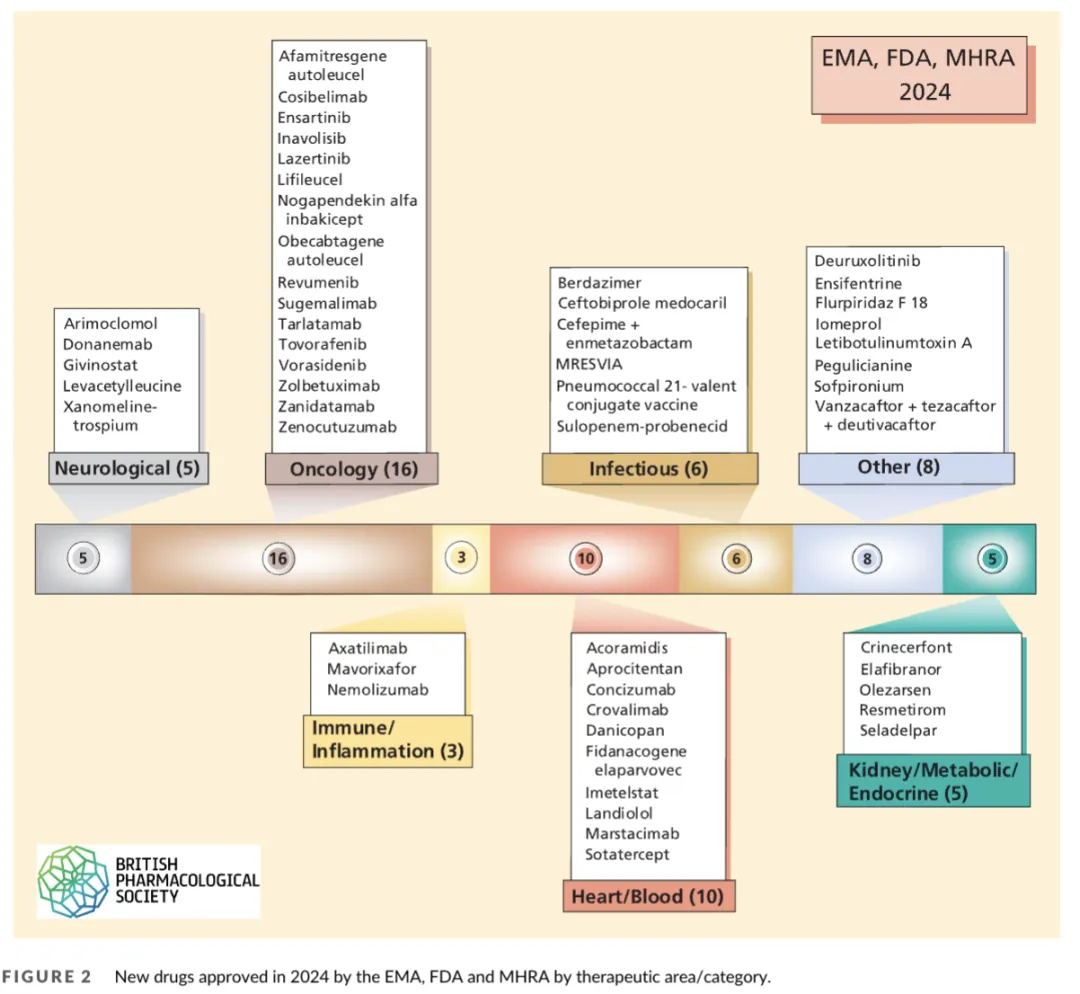
2025年4月,《British Journal of Pharmacology》(英國藥理學(xué)雜志)發(fā)布年度重磅綜述,深度解析2024年歐洲藥品管理局(EMA)、美國FDA和英國MHRA三大機構(gòu)批準(zhǔn)的53款新藥。盡管總數(shù)較2023年(70款)有所回落,但亮點頻現(xiàn):21款孤兒藥和28款全球首創(chuàng)(FIC)藥物表現(xiàn)突出,靶向機制的創(chuàng)新突破與罕見病治療的全面發(fā)力成為兩大核心方向。本文帶您全景式解讀年度新藥“成績單”,探討精準(zhǔn)醫(yī)療如何突破“無藥可治”瓶頸,為患者帶來新希望。

三大關(guān)鍵數(shù)據(jù)
53款新藥獲批
2024年,三大機構(gòu)共批準(zhǔn)53款新藥,涵蓋小分子(30款)、蛋白質(zhì)/抗體(15款)、先進療法(ATMPs,6款)及疫苗(2款)。其中孤兒藥占比高達40%(21款),罕見病治療領(lǐng)域持續(xù)升溫。
28款全球首創(chuàng)(FIC)
首次針對特定靶點或機制的創(chuàng)新藥物占比達53%,包括首個“對接-阻斷”抗體、新型精神分裂癥藥物等,多項治療領(lǐng)域?qū)崿F(xiàn)“零突破”。
區(qū)域?qū)徟町?/strong>
FDA批準(zhǔn)29款,EMA批準(zhǔn)18款,MHRA批準(zhǔn)13款。EMA對阿爾茨海默病藥物lecanemab的“先拒后批”決策引發(fā)行業(yè)對風(fēng)險評估標(biāo)準(zhǔn)的廣泛討論。

1. 腫瘤治療:從“精準(zhǔn)打擊”到“細胞革命”
實體瘤細胞療法破冰
Lifileucel(美國FDA):全球首款用于實體瘤的腫瘤浸潤淋巴細胞(TIL)療法,通過從患者腫瘤中提取并擴增T細胞后回輸,使晚期黑色素瘤患者的客觀緩解率達31.4%,中位緩解持續(xù)時間超過27個月。
Afamitresgene autoleucel(美國FDA):首個靶向MAGE-A4抗原的TCR-T細胞療法,針對滑膜肉瘤患者緩解率達37%,為軟組織肉瘤治療帶來新希望。
機制創(chuàng)新藥物
Zenocutuzumab(美國FDA):全球首個“對接-阻斷”雙特異性抗體,通過結(jié)合HER2與HER3阻斷NRG1融合致癌信號,覆蓋肺癌、胰腺癌等難治性腫瘤。
Imetelstat(美國FDA):首個端粒酶抑制劑,通過抑制癌細胞端粒延長,使39.8%的骨髓增生異常綜合征患者擺脫輸血依賴,開辟“基因?qū)用婵拱?rdquo;新賽道。
2. 罕見病:從“孤兒”到“曙光”
神經(jīng)罕見病雙藥獲批
Arimoclomol(美國FDA):聯(lián)合miglustat治療Niemann-Pick病,通過誘導(dǎo)熱休克蛋白保護神經(jīng)細胞,延緩病情進展65%,填補超罕見病治療空白。
Levacetylleucine(美國FDA):首個通過改善線粒體功能治療神經(jīng)退行性疾病的藥物,24周內(nèi)使患者共濟失調(diào)評分降低1.97分,提供代謝調(diào)控新策略。
代謝疾病突破
Olezarsen(美國FDA):首款靶向載脂蛋白CIII的反義寡核苷酸,使家族性乳糜微粒血癥患者甘油三酯水平下降43.5%,急性胰腺炎年均發(fā)作次數(shù)從11次降至1次。
3. 免疫與炎癥:從“抑制”到“精準(zhǔn)調(diào)控”
瘙癢癥特效藥
Nemolizumab(美國FDA):全球首個IL-31受體拮抗劑,針對結(jié)節(jié)性癢疹的瘙癢緩解率達56.3%,打破“抓撓-結(jié)節(jié)”惡性循環(huán),改寫頑固性瘙癢治療指南。
移植并發(fā)癥新解
Axitilimab(美國FDA):靶向CSF-1R阻斷巨噬細胞活化,使慢性移植物抗宿主病總緩解率達74%,顯著改善造血干細胞移植患者的生存質(zhì)量。
4. 心腦血管:從“替代”到“機制革新”
血友病治療范式轉(zhuǎn)變
Marstacimab(美國FDA):首款不依賴凝血因子補充的藥物,通過抑制TFPI恢復(fù)Xa因子活性,使血友病A/B患者年化出血率降低92%,實現(xiàn)從“每周注射”到“皮下長效給藥”的轉(zhuǎn)變。
高血壓耐藥突破
Aprocitentan(歐盟EMA):首個雙重內(nèi)皮素受體拮抗劑,使難治性高血壓患者收縮壓額外降低3.8 mmHg,為約10%的“藥物抵抗型”患者提供全新治療選擇。
5. 精神疾病:30年靶點新突破
Xanomeline-trospium(美國FDA):首個針對M1/M4毒蕈堿受體的激動劑組合,通過激活大腦特定受體改善精神分裂癥癥狀,5周內(nèi)使患者陽性/陰性癥狀評分降低30%,且無傳統(tǒng)抗精神病藥物的代謝副作用,被譽為“30年來該領(lǐng)域最大突破”。
6. 疫苗領(lǐng)域:mRNA技術(shù)再拓新版圖
MRESVIA(美國FDA):繼新冠疫苗后首款mRNA疫苗,針對呼吸道合胞病毒(RSV),在60歲以上人群中的預(yù)防有效率達78.7%,為通用型mRNA疫苗研發(fā)奠定基礎(chǔ)。
這些突破性藥物不僅展示了精準(zhǔn)醫(yī)療的強大潛力,也為攻克“無藥可治”的醫(yī)學(xué)難題提供了全新解決方案。
三、監(jiān)管爭議與行業(yè)啟示:從“風(fēng)險博弈”到“全球協(xié)同”
兩大焦點事件
1、Lecanemab審批“反轉(zhuǎn)劇”
美國FDA(2023年)和英國MHRA(2024年)先后批準(zhǔn)lecanemab用于早期阿爾茨海默病治療。盡管該藥可能引發(fā)20%-40%患者出現(xiàn)腦腫脹(ARIA)風(fēng)險,但歐洲藥品管理局(EMA)在“風(fēng)險-獲益”評估中最初拒絕批準(zhǔn),最終于2024年11月“反轉(zhuǎn)”批準(zhǔn)。這一事件凸顯了全球監(jiān)管機構(gòu)在“療效 vs 安全性”上的動態(tài)平衡考量。
2、孤兒藥政策傾斜
2024年批準(zhǔn)的21款孤兒藥中,15款通過FDA的“優(yōu)先審評”或“突破療法”通道加速獲批。例如,治療白血病的Revumenib僅用8個月完成審批,體現(xiàn)了“以患者為中心”的監(jiān)管創(chuàng)新。
行業(yè)啟示
機制創(chuàng)新為王
雙特異性抗體(10款)、基因與細胞療法(6款)成為研發(fā)熱點,“一藥多靶”“精準(zhǔn)靶向”成為攻克難治性疾病的關(guān)鍵路徑。
罕見病不再“罕見”
隨著基因測序和個體化醫(yī)療的進步,孤兒藥研發(fā)的回報率顯著提升。預(yù)計未來五年,全球罕見病藥物市場的年復(fù)合增長率將超過15%。
結(jié)語:當(dāng)“無藥可治”成為過去
2024年的53款新藥不僅是數(shù)字,更是千萬患者的“生命密碼”。從實體瘤細胞療法的“抗癌革命”,到罕見病藥物的“精準(zhǔn)破局”,再到精神疾病治療的“靶點破冰”,人類正以前所未有的速度突破疾病邊界。正如文章作者Stavros Topouzis所言:“這些創(chuàng)新不僅改寫指南,更預(yù)示著‘疾病agnostic’治療時代的到來——未來,藥物或?qū)⒉辉倬窒抻诓》N,而是針對共同的分子缺陷,讓更多‘絕癥’變?yōu)?lsquo;可控慢性病’。”
數(shù)據(jù)來源與期刊背景
本文數(shù)據(jù)來源于《British Journal of Pharmacology》2025年4月綜述“Novel drugs approved by the EMA, the FDA and the MHRA in 2024: A year in review”。《British Journal of Pharmacology》:藥理學(xué)領(lǐng)域的“年度風(fēng)向標(biāo)”,創(chuàng)刊于1908年,專注于藥物作用機制、新藥發(fā)現(xiàn)及監(jiān)管科學(xué),最新影響因子為7.7(2023年)。其年度新藥綜述因覆蓋三大機構(gòu)、深度解析機制創(chuàng)新,已成為全球醫(yī)藥行業(yè)、監(jiān)管機構(gòu)及臨床醫(yī)生的“決策參考手冊”。
標(biāo)簽:
創(chuàng)新藥
- 磁珠自動化純化系統(tǒng)的優(yōu)勢及在抗體表征分析IgG抗體藥物研發(fā)中的應(yīng)用
- 雙特異性抗體的作用機制及在重塑腫瘤靶向治療中的應(yīng)用及挑戰(zhàn)
- 一步法ELISA檢測的原理、靶標(biāo)、影響因素及優(yōu)化方法
- His標(biāo)簽蛋白純化技術(shù)的原理、優(yōu)勢及在生物醫(yī)學(xué)研究中的應(yīng)用
- 第三代ADC藥物在突破實體瘤治療瓶頸中的策略與創(chuàng)新體現(xiàn)
- FMC63抗體的質(zhì)量控制標(biāo)準(zhǔn)及在CAR-T檢測和治療中的應(yīng)用優(yōu)勢
- 流式抗體染色操作流程(含表面/胞內(nèi))
- IHC抗體在癌癥生物標(biāo)志物檢測中的選擇原則及應(yīng)用
Copyright(C) 1998-2025 生物器材網(wǎng) 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






